
分析 (1)酸或碱都抑制水电离,能水解的盐促进水解,不水解的盐对水的电离无影响,依此进行判断;
(2)依据选项中提供的反应信息判断,LiH燃烧是和氧气反应生成产物为Li2O(S)+H2O(l),结合热化学方程式和盖斯定律,通过合并热化学方程式得到所求的热化学方程式,注意热化学方程式改变系数,焓变随之改变;
(3)根据该反应的物质种类和状态均不变来分析.
解答 解:(1)酸或碱都抑制水电离,故②NaOH和③H2SO4溶液中水的电离程度较小,由于硫酸是二元强酸,氢氧化钠是一元强碱,故相同物质的量浓度的硫酸中水的电离程度小于氢氧化钠中水的电离程度;能水解的盐促进水解,故④(NH4)2SO4溶液中水的电离程度最大;不水解的盐①NaCl对水的电离无影响,
故水的电离程度的正确排列顺序为:④>①>②>③.
故答案为:④>①>②>③;
(2)①2Li(S)+H2(g)═2LiH(s)△H=-182kJ•mol-1;
②2H2(g)+O2(g)═2H2O(1)△H=-572kJ•mol-1;
③4Li(s)+O2(g)═2Li2O(s)△H=-1196kJ•mol-1,
依据热化学方程式结合盖斯定律③-①×2+③得到:
4LiH(s)+2O2(g)=2Li2O(s)+2H2O(l)△H=-14O4KJ/mol,
即热化学方程式为2LiH(s)+O2(g)═Li2O(S)+H2O(l)△H=-702 kJ•mol;
故答案为:2LiH(s)+O2(g)═Li2O(S)+H2O(l)△H=-702 kJ•mol;
(3)由于该反应的物质种类和状态均不变,故该反应是熵变△S=0的反应,该反应在高温下能自发进行,故答案为:=,能自发进行.
点评 本题考查了酸碱盐对水的电离的影响和盖斯定律的运用,难度不大,应注意的是酸和碱均抑制水的电离,盐的水解促进水的电离.


科目:高中化学 来源: 题型:选择题
| A. | 1molC质量是12 g•mol-1 | |
| B. | 22.4L H2的物质的量是1mol | |
| C. | 将60gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度是1.5mol•L-1 | |
| D. | NaCl的摩尔质量是58.5 g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
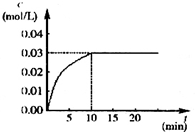 在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g);△H>0反应中CO2的浓度随时间变化情况如下图:
在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g);△H>0反应中CO2的浓度随时间变化情况如下图:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 材料的不断发展可以促进社会进步.
材料的不断发展可以促进社会进步.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com