
| A. | ①② | B. | ③④ | C. | ①③④ | D. | ①②③④ |
分析 ①由于重水的离子积常数为1.6×10-15,重水中[D+]=4×10-8,再根据pD=-lg[D+]计算;
②在0.01mol/LNaOD溶液中[OD-]=0.01mol/L,根据重水离子积常数,可推知[D+]=1.6×10-13mol/L,再根据pD=-lg[D+]计算;
③在0.01mol/L的DCl的重水溶液中[D+]=0.01mol/L,再根据pD=-lg[D+]计算;
④根据中和反应量的关系,100mL 0.25mol/L DCl和50mL 0.2mol/L NaOD中和后溶液中DCl过量,计算剩余DCl浓度,再根据pD=-lg[D+]计算.
解答 解:①由于重水的离子积常数为1.6×10-15,重水中c(D+)=c(OD-)=$\sqrt{1.6×1{0}^{-15}}$mol•L-1=4×10-8 mol•L-1,根据pD=-lg[D+]=-lg4×10-8=7.4>7.0,故正确;
②在1LD2O中,溶解0.01molNaOD,则溶液中[OD-]=0.01mol/L,根据重水离子积常数,可知[D+]=$\frac{1.6×1{0}^{-15}}{0.01}$mol/L=1.6×10-13mol/L,pD=-lg[D+]=-lg1.6×10-13=13-lg1.6≠12,故错误;
③在0.01mol/L的DCl的重水溶液中[D+]=0.01mol/L,pD=-lg[D+]=-lg0.01=2,故正确;
④根据中和反应量的关系,100mL 0.25mol/L DCl和50mL 0.2mol/L NaOD中和后溶液中DCl过量,剩余DCl浓度为$\frac{100mL×0.25mol/L-50mL×0.2mol/L}{100mL+50mL}$=0.1mol/L,则[D+]=0.1mol/L,故pD=-lg[D+]=-lg0.1=1,故正确,
故选:C.
点评 本题以给予pD情景为载体,考查溶液pH有关计算,注意把水的离子积和溶液pH知识迁移过来,侧重考查处理新情景问题能力.


科目:高中化学 来源: 题型:选择题
| A. | 水银、硫酸、烧碱、硫酸氢钠 | B. | 氯水、盐酸、火碱、硫酸钡 | ||
| C. | 臭氧、硝酸、纯碱、胆矾 | D. | 铜、醋酸、石灰石、氯化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
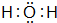 、
、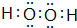 (用元素符号表示)
(用元素符号表示)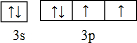 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 节假日期间,在开阔的广场燃放烟花爆竹 | |
| B. | 进入煤矿井时,用火把照明 | |
| C. | 实验时,将水倒入浓硫酸配制稀硫酸 | |
| D. | 用点燃的火柴在液化气钢瓶口检验是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 d.CH2=CHCH3.
d.CH2=CHCH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | N2(g)+3H2(g)?2NH3(g)△H=-Q1 kJ•mol-1 (Q1>0) | |
| B. | 2SO3(g)?2SO2(g)+O2(g)△H=+Q2 kJ•mol-1 (Q2>0) | |
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-Q3 kJ•mol-1 (Q3>0) | |
| D. | H2(g)+CO(g)?C(s)+H2O(g)△H=+Q4 kJ•mol-1 (Q4>0) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取 | B. | 过滤 | C. | 蒸馏 | D. | 蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰石在高温下的分解反应 | B. | 生石灰和水的反应 | ||
| C. | 盐酸与氢氧化钠溶液的反应 | D. | 木炭在氧气中燃烧 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com