
| 物质 | MnS | CuS | PbS |
| Ksp | 2.5×10-13 | 6.3×10-36 | 8.0×10-28 |
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
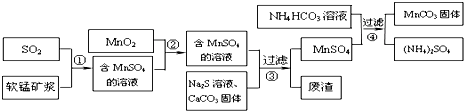
分析 软锰矿主要成分为MnO2,其中含有铁、铝、硅的氧化物和少量重金属化合物杂质,用软锰矿与来自工业废气主要是SO2反应生成硫酸锰,另外还原硫酸铁、硫酸亚铁等,再加入二氧化锰反应使亚铁离子被氧化成铁离子,得到含有硫酸锰的溶液中再加入硫化钠和碳酸钙固体,反应后过滤得硫酸锰溶液,在硫酸锰溶液中加入碳酸氢钠得碳酸锰沉淀和硫酸铵溶液,过滤得碳酸锰固体,
(1)软锰矿浆是二氧化锰,MnSO4溶液水解显酸性,Fe3+将SO2氧化为硫酸;
(2)MnO2可将Fe2+氧化成Fe3+,Fe3+完全沉淀的pH较Fe2+低;
(3)碳酸钙与溶液中的H+反应,使溶液中的PH升高;
(4)加入一种反应物能提高另一种反应物的装化率;MnCO3,NH4HCO3与酸反应;
(5)锰矿与煤炭粉混合,焙烧生成二氧化硫,污染空气.
解答 解:(1)软锰矿浆是二氧化锰,MnSO4溶液水解先酸性,根据2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.Fe3+可将SO2氧化为硫酸,故答案为:小;工业制备硫酸;
(2)MnO2可将Fe2+氧化成Fe3+,反应的离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,Fe3+完全沉淀的pH较Fe2+低,所以将溶液中的Fe2+氧化成Fe3+,
故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;使Fe2+ 转变为Fe3+,Fe3+完全沉淀的pH较低(或Fe3+更易沉淀);
(3)碳酸钙与溶液中的H+反应,使溶液中的PH升高,使溶液中的Fe3+、Al3+转化为氢氧化物沉淀,
故答案为:与溶液中的酸反应,使溶液中的Fe3+、Al3+转化为氢氧化物沉淀;
(4)加入稍过量的NH4HCO3能提高MnSO4的装化率,使MnCO3沉淀完全,溶液的pH不过低,H+可与MnCO3,NH4HCO3反应,
故答案为:使MnCO3沉淀完全;MnCO3沉淀量少,NH4HCO3与酸反应(或MnCO3、NH4HCO3与酸反应溶解);
(5)锰矿与煤炭粉混合,焙烧生成二氧化硫,污染空气,而工艺A不仅不产生二氧化硫,且能生产硫酸,故答案为:节约能源、治理含SO2的工业废气等.
点评 本题考查了流程分析,反应过程理解应用,反应现象和产物的判断,注意基本实验的操作步骤,离子方程式书写等,题目难度中等.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的能量一定高于N | |
| B. | X、Y的能量总和高于M、N的能量总和 | |
| C. | 因为该反应为放热反应,故不必加热就可发生 | |
| D. | 断裂X、Y的化学键所吸收的能量高于形成M、N的化学键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF电离:HF(aq)?H+(aq)+F-(aq)△H=+10.4kJ/mol | |
| B. | 水解消耗0.1mol F-时,吸收的热量为6.77kJ | |
| C. | 中和热均为57.3 kJ/mol | |
| D. | 含0.1mol HF、0.1mol NaOH 的两种溶液混合后放出的热量为6.77kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质在酶的作用下水解的最终产物为氨基酸 | |
| B. | 向蛋白质溶液加入(NH4)2SO4浓溶液,会使其变性 | |
| C. | 天然蛋白质仅由碳、氢、氧、氮四种元素组成 | |
| D. | 氨基酸和蛋白质都是只能和碱反应的酸性物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com