
【题目】稀土元素号称“工业维生素”,科学家把稀土元素镧对作物的作用赋予“超级钙”的美称.已知镧(La)是一种活动性比锌更强的元素,它的氧化物的化学式为La2O3 , La(OH)3是不溶于水的弱碱,而LaCl3、La(NO3)3都可溶于水,下列说法中正确的是( )
A.La(NO3)3水溶液显酸性
B.LaCl3的水溶液加热蒸发灼烧,最终得到无水LaCl3
C.La和盐酸反应的离子方程式为:La+2H+=La3++H2↑
D.镧有两种核素: ![]() 和放射性
和放射性 ![]() ,由此可知镧元素的相对原子质量为138.5
,由此可知镧元素的相对原子质量为138.5
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】奈必洛尔是一种用于血管扩张的降血压药物.用于合成奈必洛尔中间体G的部分流程如图: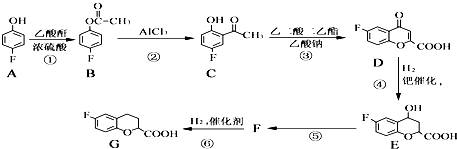
已知:乙酸酐的结构简式为 ![]() 请回答下列问题:
请回答下列问题:
(1)G物质中的官能团的名称是羧基,、 .
(2)反应A→B的化学方程式为 .
(3)上述④、⑤变化过程的反应类型分别是、 .
(4)写出满足下列条件的C的同分异构体的结构简式:、Ⅰ.苯环上只有两种取代基.Ⅱ.分子中只有4种不同化学环境的氢.
Ⅲ.能与NaHCO3反应生成CO2 .
(5)根据已有知识并结合相关信息,写出以 ![]() 和乙酸酐为原料制备
和乙酸酐为原料制备 ![]() 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)在200mL2molL﹣1 AlCl3溶液中,溶质的物质的量为 . 此溶液中Al3+的物质的量浓度为 , Cl﹣的物质的量浓度为 .
(2)分析下列氧化还原反应,指出氧化剂和还原剂、氧化产物和还原产物.CuO+CO ![]() Cu+CO2还原剂: , 氧化剂 ,
Cu+CO2还原剂: , 氧化剂 ,
还原产物: , 氧化产物 ,
(3)分别取0.1mol镁、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与实验相关的叙述正确的是( )
A.稀释浓硫酸时,应将蒸馏水沿烧杯内壁缓慢地注入浓硫酸中并不断搅拌
B.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
C.配制1molL﹣1 300mL NaCl溶液可以选择一个50mL的容量瓶和一个250mL的容量瓶
D.可以用如图装置进行氯气的尾气处理 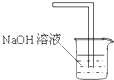
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验. 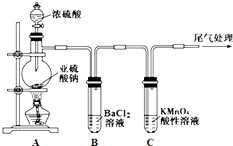
已知:Na2SO3+H2SO4(浓) ![]() Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是 .
(2)实验过程中,C中的现象是 , 说明SO2具有性.
(3)实验过程中,观察到装置B中出现了明显的白色沉淀.为探究该白色沉淀的成分,该小组同学进行了如下实验: ![]()
根据实验事实判断该白色沉淀的成分是(填化学式),产生该白色沉淀的原因可能是(填字母编号).
a.BaSO3既不溶于水也不溶于酸 b.BaCl2溶液中可能溶解有氧气
c.BaCl2溶液中可能混有NaOH d.由A制得的SO2气体中可能混有氧气
(4)如果将装置A中的浓H2SO4换作浓HNO3 , 对此实验是否有影响并明理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,下列选项中括号内的物质能被完全消耗的是( )
A.常温下将64g铜片投人过量浓硫酸中(铜片)
B.向含有0.2molBa(OH)2和0.lmolNaOH的混合溶液中通人标况下3.36LCO2(CO2)
C.向l0mL3molL﹣1的盐酸中加人5.6g铁(铁)
D.向5.5gMnO2粉末中加人20mL2molL﹣1双氧水(MnO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO的应用和治理问题属于当今社会的热点问题.
(1)汽车尾气中CO的治理,常用四氧化三钴(Co3O4)纳米棒的作催化剂,低温下与O2反应生成CO2 . 下列说法中正确的是(不定项选择)
A.该反应是分解反应
B.反应前后Co3O4化学性质不改变
C.反应前后碳元素的化合价不变
D.该反应的△H<0
(2)光气(COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)COCl2(g)制备.左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线.回答下列问题: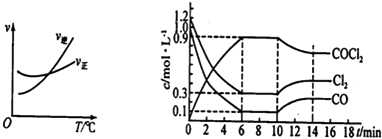
①0~6min内,反应的平均速率v(Cl2)=;
②若保持温度不变,在第8min加入体系中的三种物质各1mol,则平衡移动(填“向正反应方向”、“向逆反应方向”或“不”);
③若将初始投料浓度变为c(Cl2)=0.8mol/L、c(CO)=0.6mol/L、c(COCl2)=mol/L,保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同;
④该反应的平衡常数的表达式为K= , 随温度升高,该反应平衡常数变化的趋势为(填“增大”、“减小”或“不变”),原因为⑤比较第8min反应温度T(8)与第15min反应温度T(15)的高低:T(8)T(15)(填“<”、“>”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol H2SO4的质量为98gmol-1 B. SO3的摩尔质量为80gmol-1
C. 1molO就是1mol 氧气 D. SO2 的摩尔质量与其相对分子质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
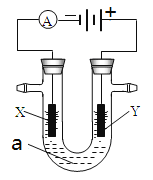
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应是______________。在X极附近观察到的现象是______________________________。
②Y电极上的电极反应式是______________。检验该电极反应产物的方法是______________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是___________________,电极反应式是______________。
②Y电极的材料是___________________,电极反应式是______________。
(说明:杂质发生的电极反应不必写出)
③假若电路中有0.04摩尔电子通过时,阴极增重________克。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com