
| a |
| x |
| 1 |
| 3 |
| 7 |
| 30 |
| ||
|
| 0.7mol-3n(Al3+) |
| 2 |
| 0.7mol-3×0.1mol |
| 2 |
| 0.1mol |
| 0.1mol+0.2mol+0.7mol |
| 0.7mol-3a |
| 2 |
| a |
| x |
| 0.7mol-3a |
| 2 |
| a |
| x |
| 2.1x |
| x+2 |
| 2.1x |
| x+2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图有机物具有多种官能团,因而能跟多种物质反应,但因其分子内的羧基与醇羟基、酚羟基间“位阻”较大,故不能发生分子内的酯化反应,试写出该有机物发生下列反应的方程式:
如图有机物具有多种官能团,因而能跟多种物质反应,但因其分子内的羧基与醇羟基、酚羟基间“位阻”较大,故不能发生分子内的酯化反应,试写出该有机物发生下列反应的方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
 50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题.
50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
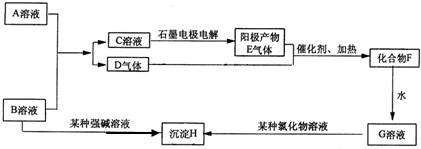
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com