
某温度下,将0.2 mol C(s)和0.3 mol H2O(g),投入2 L的密闭容器中,发生反应C(s)+H2O(g) CO(g)+H2(g),5 min达到平衡后,密度增加了0.3 g·L-1。有关下列说法正确的是
CO(g)+H2(g),5 min达到平衡后,密度增加了0.3 g·L-1。有关下列说法正确的是
A.从反应开始到平衡过程中,用C来表示该反应的平均速率为0.005 mol·L-1·min-1
B.达平衡时压强变为原来的7/6
C.此温度下该反应的平衡常数为0.005
D.若保持温度和体积不变,向平衡体系中再加入0.2 mol C(s)和0.3 mol H2O(g),重新达到平衡后,H2O的转化率等于16.7%
BC
【解析】
试题分析:A、碳是固体,不能用来表示反应速率,A不正确;B、5 min达到平衡后,密度增加了0.3 g/L,则容器中气体的质量增加了0.6g,则根据方程式C(s)+H2O(g) CO(g)+H2(g)可知增加的质量就是参加反应的碳的质量,物质的量是0.6g÷12g/mol=0.05mol,则
CO(g)+H2(g)可知增加的质量就是参加反应的碳的质量,物质的量是0.6g÷12g/mol=0.05mol,则
C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
起始量(mol) 0.3 0 0
转化量(mol) 0.05 0.05 0.05
平衡量(mol) 0.25 0.05 0.05
因此达平衡时压强变为原来的(0.25+0.05+0.05)÷0.3=7/6,B正确;
此温度下该反应的平衡常数为 =0.005,C正确;
=0.005,C正确;
若保持温度和体积不变,向平衡体系中再加入0.2 mol C(s)和0.3 mol H2O(g),相当于是增大压强,平衡向正反应方向移动,因此水蒸气的转化率将大于 ×100%=16.67%,D不正确,答案选BC。
×100%=16.67%,D不正确,答案选BC。
考点:考查可逆反应的有关计算


科目:高中化学 来源:2013-2014江苏省泰州市姜堰区高二下学期期中考试 化学试卷(解析版) 题型:填空题
(18分)运用物质结构的知识完成下列问题。
(1)第一电离能介于B、N之间的第二周期元素有 (填元素符号)。
(2)配离子[TiCl(H2O)5]2+的中心离子化合价为 ,配体的化学式为 。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:

Q R
①晶体Q中不存在的作用力为 (填字母)。
A.共价键 B.离子键 C.配位键 D.范德华力 E.氢键
②R中阳离子的空间构型为 。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm—(含B、O、H三种元素)的球棍模型如下图3所示。则m= (填数字)。
(5)以四氯化钛、碳化钙、叠氮酸盐(如NaN3)作原料,可以生成碳氮化钛化合物,其结构是用碳原子取代氮化钛晶胞(结构如下图4)所有顶点的氮原子,这种碳氮化钛化合物的化学式为 。
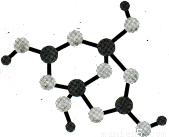
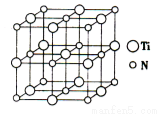
图3 图4
(6)部分化学键的键能见下表:
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/ kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
①比较下列两组物质的熔点高低 (填“>”或“<”) SiC______ Si; SiCl4 ______ SiO2
②工业上高纯硅可通过下列反应制取:SiCl4 (g) + 2H2(g) 高温Si(s) + 4HCl(g)
计算该反应的反应热△H =___________ kJ/mol。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省无锡市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A.SO2和Si B.CO2和H2O
C.NaCl和HCl D.CCl4和KCl
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高一期末模拟化学试卷(解析版) 题型:选择题
小华家中有如下生活用品:碘酒、食盐、食醋、84消毒液(内含NaClO),小华利用上述用品不能完成的任务是
A.检验买来的奶粉中是否加有淀粉 B.检验自来水中是否含有Cl-
C.除去保温瓶中的水垢 D.洗去白色衣服上的番茄汁
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高二下学期阶段测试5月 化学试卷(解析版) 题型:填空题
(16分)钠及其化合物具有广泛的用途。
(1)工业上制备金属钠的常用方法是 (用离子方程式表示)。
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示:
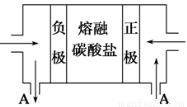
正极的电极反应式为 ,电池工作时物质A可循环使用,A物质的化学式为 。
(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 11.6 | 10.3 | 11.1 |
上述盐溶液的阴离子中,结合H+能力最强的是 ,根据表中数据,浓度均为0.01 mol·L-1下列四种酸的溶液分别稀释100倍,pH变化最大的是 (填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当300 mL 1 mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为 。
②已知几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时, (填离子符号)先沉淀,Ksp[Fe(OH)2] Ksp[Mg(OH)2](填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高二下学期阶段测试5月 化学试卷(解析版) 题型:选择题
一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如下图所示,该电池的电解质为6 mol/LKOH溶液,下列说法中正确的是
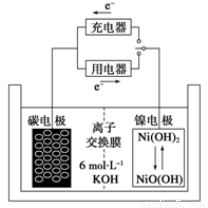
A.放电时K+移向负极
B.放电时电池负极的电极反应为H2-2e-=2H+
C.放电时电池正极的电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
D.该电池充电时将碳电极与电源的正极相连
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高二下学期阶段测试5月 化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.中子数为20的氯原子:
B.HClO的电子式: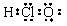
C.K2O的电子式: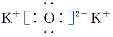
D.熔融状态下硫酸氢钾的电离方程式:KHSO4=K++H++SO
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高三模拟考试化学试卷(解析版) 题型:选择题
下列有关物质的性质或应用均正确的是
A.Si是一种非金属主族元素,其氧化物可用于制作计算机芯片
B.氢氧化镁分解时吸收大量的热量,添加到合成树脂中可作阻燃剂
C.铁具有良好的导电性,氯碱工业中可用铁作阳极电解食盐水
D.用二氧化硫加工银耳,使之更白
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省徐州市高三第三次模拟考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 25 ℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA
B. 1.2 g C60和石墨的混合物中,含有的碳原子数目为0.1NA
C. 2.24 L N2和NH3的混合气体中,含有的共用电子对数目为0.3NA
D. 标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com