
| N |
| NA |
| N |
| NA |
| 3×6.02×1023 |
| 6.02×1023mol-1 |
| 1.204×1024 |
| 6.02×1023mol-1 |


科目:高中化学 来源: 题型:
| A、氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++2OH-+2 HCO3-=CaCO3↓+CO32-+2H2O |
| C、向CuSO4溶液中加入Ba(OH)2溶液,观察到有蓝色沉淀生成:Cu2++2OH-=Cu(OH)2↓ |
| D、FeSO4溶液中加H2O2溶液:Fe2++2H2O2+4H+=Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3的电离方程式:CaCO3?Ca2++CO32- |
| B、HCO3-的水解方程式:HCO3-+H2O?H3O++CO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、BaSO4的沉淀溶解平衡表达式:BaSO4(s)?Ba2+(aq)+SO42-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaAlO2溶液中通入足量的CO2:2AlO2-+CO2+3H2O?2Al(OH)3↓+CO32- |
| B、NaHCO3溶液中滴加过量Ca(OH)2溶液:Ca2++OH-+HCO3-?CaCO3↓+H2O |
| C、硫酸铝溶液中加入过量氨水:Al3++4NH3?H2O?AlO2-+4NH4++2H2O |
| D、NaHSO4溶液中加入Ba(OH)2溶液至溶液呈中性:Ba2++OH-+H++SO42-?BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| 密度(g/mL) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 冰醋酸 | 1.049 | 16.6 | 118.1 | 能溶于水 |
| 异戊醇 | 0.812 | -117.2 | 130.5 | 微溶于水 |
| 乙酸异戊酯 | 0.869 | -78 | 140 | 难溶于水 |
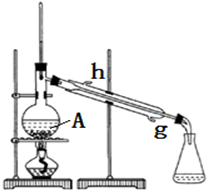
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com