
【题目】现有下列气体:H2、Cl2、CH4、HCl、NH3、NO、H2S、SO2,用如图装置进行实验,填写下列空白:
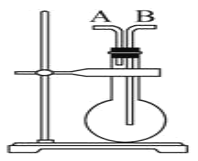
(1)当烧瓶干燥时,从A口进气可收集的气体是___________,从B口进气可收集的气体是___________。
(2)当烧瓶中充满水时,可用来测___________等气体的体积。
(3)可用启普发生器制取的气体有___________
【答案】H2、CH4、NH3 Cl2、HCl、H2S、SO2 H2、CH4、NO H2、NO 、H2S
【解析】
H2、CH4、NH3的密度小于空气的密度,Cl2、HCl、H2S、SO2 的密度大于空气,NO能与氧气反应。
(1)由于H2、CH4、NH3的密度比空气小,不与空气发生反应,可用向下排空气法来收集,结合本题干燥烧瓶导气管的位置特征,H2、CH4、NH3应从A口进气,把空气从B口赶出;Cl2、HCl、H2S、SO2气体的密度比空气大,与空气不发生反应,应从 B口进气,将空气从A口赶出;NO能与空气中的O2反应,不能用排空气法收集。
(2)对于难溶于水的气体可用排水集气法收集、测量气体的体积,H2、CH4、NO难溶于水,可用排水集气法收集、测量的气的体积。
(3)启普发生器的条件:1、块状固体和液体反应;2、不需要加热;3、生成气体不能易溶于水,所以H2、NO、H2S可用启普发生器制取。


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲溶液加入(或通入)物质乙(乙物质为气体或溶液),生成沉淀的质量与消耗乙的质量关系曲线符合图的是

A.向Na[Al(OH)4]溶液中通入二氧化碳
B.向Na[Al(OH)4]溶液中滴加盐酸
C.向澄清石灰水中通入二氧化碳
D.向Al2(SO4)3溶液中滴加NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝。工艺流程如图,下列有关说法正确的是
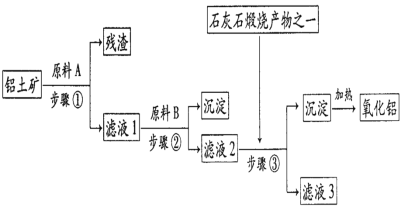
A.该流程中,原料A可以是盐酸,也可以是氢氧化钠溶液
B.步骤2 中要发生的反应有:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=[Al(OH)4] -、H++OH-=H2O
C.滤液3中的主要离子有碳酸根、钠离子、氯离子
D.工业上冶炼铝用氧化铝不用氯化铝的原因是,氧化铝是电解质,氯化铝是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质:①Ar ②Na2O2 ③AlCl3 ④HClO ⑤N2 ⑥MgF2 ⑦NH4Cl
(1)只存在共价键的是___,不存在化学键的是_____,离子化合物有_______
(2)由离子键和极性键构成的物质是__________
(3)N2的电子式为_____ HClO的电子式为________NH4Cl的电子式为___________
(4)用电子式表示MgF2的形成过程___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上乙醚可用于制造无烟火药。无水乙醚微溶于水,熔点-116.3 ℃,沸点34.6 ℃,在空气中遇热易爆炸。实验室合成乙醚的原理如下:
主反应:2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
副反应:CH3CH2OH![]() H2C=CH2↑+H2O
H2C=CH2↑+H2O
(乙醚制备)装置设计如图所示(部分装置略):

(1)仪器b应更换为下列中的________(填字母代号)。
A.干燥器
B.直形冷凝管
C.玻璃管
D.安全瓶
(2)实验操作的正确排序为________(填字母代号),取出乙醚立即密闭保存。
a.安装实验仪器 b.加入12 mL浓硫酸和少量乙醇的混合物
c.检查装置气密性 d.熄灭酒精灯
e.通冷却水并加热烧瓶 f.拆除装置
g.控制滴加乙醇速率与馏出液速率相等
(3)反应温度不超过145 ℃,其目的是____________________。
(乙醚提纯)
![]()
(4)操作a的名称是__________;进行该操作时,必须用水浴加热代替酒精灯加热,其目的与制备实验中将尾接管支管通入室外相同,均为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol·L-1的氢氧化钠溶液,生成的沉淀跟加入的氢氧化钠溶液的体积关系如图(横坐标体积单位是mL,纵坐标质量单位是g)。
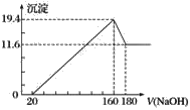
(1)合金中镁的质量是__________。
(2)所用盐酸的物质的量浓度是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1 mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知![]() ]。下列叙述不正确的是( )
]。下列叙述不正确的是( )
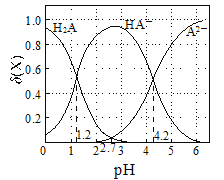
A.NaHA溶液中,HA-的水解能力小于HA-的电离能力
B.lg[K2(H2A)]=-4.2
C.将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)
D.0.1 mol·L1 NaHA溶液中:c(Na+)+c(A2)+c(H2A)+c(HA)=0.2 mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
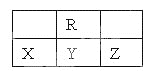
A. X的氢化物比R的氢化物稳定
B. 原子半径大小顺序是Z>Y>X
C. Y、R形成的化合物YR2能使KMnO4溶液褪色
D. X、Z可形成化合物XZ5 , 分子中各原子均满足最外层8电子结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com