
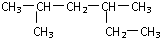 的名称是2,4-二甲基己烷
的名称是2,4-二甲基己烷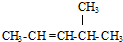 的名称是2-甲基-2-戊烯
的名称是2-甲基-2-戊烯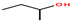
分析 (1)最长碳链有6个碳原子;
(2)从距离双键近的一端命名;
(3)键线式用线段表示化学键,端点、交点为碳原子,碳原子、H原子不需要标出,杂原子及杂原子上的H原子需要标出;
(4)CH2=CH-CH=CH2与溴单质发生1,4-加成,2个双键均断裂,在中间形成1个新的双键;
(5)乙炔是直线型分子,甲烷是正四面体结构.
解答 解:(1)最长碳链有6个碳原子,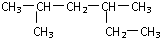 的名称是2,4-二甲基己烷,故答案为:2,4-二甲基己烷;
的名称是2,4-二甲基己烷,故答案为:2,4-二甲基己烷;
(2)从距离双键近的一端命名,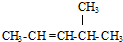 的名称是2-甲基-2-戊烯故答案为:2-甲基-2-戊烯;
的名称是2-甲基-2-戊烯故答案为:2-甲基-2-戊烯;
(3)含有羟基为醇类,含有羟基的最长碳链为4,距离羟基最近的一端为1号碳,故2-丁醇的键线式为 ,故答案为:
,故答案为: ;
;
(4)CH2=CH-CH=CH2与溴单质发生1,4-加成,2个双键均断裂,在中间形成1个新的双键,反应为CH2=CH-CH=CH2+Br2→BrCH2CH=CHCH2Br,
故答案为:CH2=CH-CH=CH2+Br2→BrCH2CH=CHCH2Br;
(5)乙炔是直线型分子,取代乙炔中氢原子的碳在同一直线上,最多有3个碳原子在一条直线上,故答案为:3.
点评 本题考查了有机物的命名方法的应用、键线式和加成反应、有机物的结构等,题目难度中等,注意主链选择,位置编号的正确选择和加成反应的原理.


科目:高中化学 来源: 题型:填空题
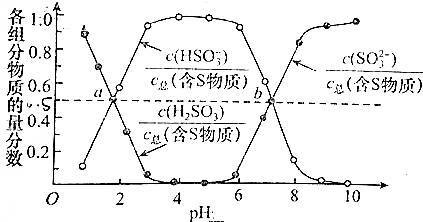
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH 4 | B. | C 2H 4 | C. | C 2H 6O | D. | C 6H 12O 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、MnO4-、NO3- | B. | Fe3+、A13+、Cl-、HS- | ||
| C. | NH4+、AlO2-、Na+、CH3COO- | D. | K+、Na+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4不能从中萃取出碘 | |
| B. | 将3~4个火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素 | |
| C. | 硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 | |
| D. | 提取海带中碘元素时,为保证I-完全氧化为I2,加入的氧化剂(H2O2或新制氯水)均应过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
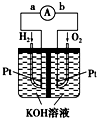 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
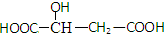 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 1mol苹果酸可与3mol NaOH发生中和反应 | |
| B. | 苹果酸中能发生酯化反应的官能团有2种 | |
| C. | 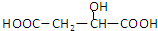 与苹果酸互为同分异构体 与苹果酸互为同分异构体 | |
| D. | 1mol苹果酸与足量金属Na反应生成生成1mol H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com