
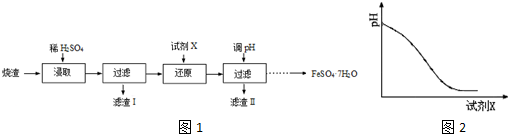
分析 烧渣中加入稀硫酸,得到硫酸铁、硫酸亚铁和硫酸铝,二氧化硅不反应,过滤,滤渣Ⅰ为二氧化硅,在滤液中加入试剂X,随着X的加入,溶液pH逐渐减小,X应为SO2,得到硫酸铝和硫酸亚铁溶液,调节溶液pH,生成氢氧化铝沉淀,滤渣Ⅱ为氢氧化铝,溶液经蒸发结晶、过滤、洗涤、干燥,可得到FeSO4•7H2O,以此解答该题.
解答 解:烧渣中加入稀硫酸,得到硫酸铁、硫酸亚铁和硫酸铝,二氧化硅不反应,过滤,滤渣Ⅰ为二氧化硅,在滤液中加入试剂X,随着X的加入,溶液pH逐渐减小,X应为SO2,得到硫酸铝和硫酸亚铁溶液,调节溶液pH,生成氢氧化铝沉淀,滤渣Ⅱ为氢氧化铝,溶液经蒸发结晶、过滤、洗涤、干燥,可得到FeSO4•7H2O,
(1)溶液中的Fe2+易被空气中的O2氧化,反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,提高烧渣浸取速率,可增大固体的表面积,提高反应温度,或增大浓度,只有AC符合,
故答案为:4Fe2++O2+4H+=4Fe3++2H2O;AC;
(2)由以上分析可知,溶液酸性增强,应通入二氧化硫,被氧化生成硫酸,反应后溶液中含有SO42-,故答案为:B;SO42-;
(3)由以上分析可知滤渣Ⅱ为氢氧化铝,即Al(OH)3,溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得到FeSO4•7H2O,
故答案为:Al(OH)3;蒸发浓缩;冷却结晶.
点评 本题考查化学实验制备方案设计,为高频考点,涉及盐类水解、氧化还原反应等知识点,明确反应原理及物质性质是解本题关键,熟悉流程图中发生的反应及基本操作方法,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N原子在同一周期(或电子层数相同),N原子核电荷数更大,原子半径更小,原子核对外层电子的吸引力更强.
),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N原子在同一周期(或电子层数相同),N原子核电荷数更大,原子半径更小,原子核对外层电子的吸引力更强.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 刚玉(Al2O3)、金刚砂(SiC)等是耐高温材料 | |
| B. | 氨和二氧化硫易液化,可通过氨水分解吸热,使周围温度降低,可做制冷剂 | |
| C. | 浓硫酸可用于干燥SO2、NO2等气体 | |
| D. | 硅酸钠的水溶液是制备硅胶和木材防火剂的原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com