
����Ŀ���̷�(FeSO4��7H2O)������ȱ����ƶѪҩƷ����Ҫ�ɷ֡��������������������������������������ʣ�Ϊԭ�����������̷���һ�ַ�����
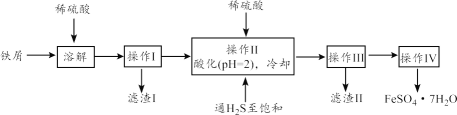
��֪�������±���H2S��Һ��pHԼΪ3.9��SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0��������ȫʱ��pHΪ5.5��
��1����ҵ�����ù���ϡ�����ܽ���м����������Ⱦ�����壬�䷴Ӧ���ӷ���ʽ��_____��
��2������II�У�ͨ�����������͵�Ŀ����_________������Һ���������ữ��pH=2��Ŀ����_____��
��3�������£�Ksp[Fe(OH)3]=4.0��10-38����Fe3+��ˮ�ⳣ��Ϊ_____��
��4������IV�õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ�����ȥ������渽�ŵ���������ʣ���_____��
��5�����õ��̷�(FeSO4��7H2O)��������O2��������������Fex(OH)y(SO4)z��wH2O���ֲⶨ����ɣ��������£��������ʲ����뷴Ӧ����ÿ����Ӧ����ȫ���У���
��ȡ���ȷݹ�����Ʒ��
��һ����Ʒ������ϡ�����ܽ����250mL����ƿ�ж��ݣ���ȡ25.00mL������Һ����ƿ�У���0.03mol/LKMnO4��Һ�ζ����յ㣬����KMnO4��Һ���Ϊ20.00mL���ζ�ʱ��Ӧ�����ӷ���ʽΪ��5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O�����ζ�����Һ������pH����Fe3+�����ˡ�ϴ�ӡ���ɲ����գ����յõ�0.32gFe2O3��(Fe2O3ʽ��160)
�ڶ�����Ʒ������ϡ�����ܽ���ټ������BaCl2��Һ�������ˡ�ϴ�ӡ���ɣ���9.32gBaSO4������(BaSO4ʽ��233)
��������Ʒ�����³�����պ��ռ���4.05gH2O�����Ƶ�������(Fex(OH)y(SO4)z��wH2O)�Ļ�ѧʽ��д��������̣�x��y��z��wΪ��������ȣ�______________________________________________________��
���𰸡�3Fe+8H�� +2NO3��=3Fe2�� +2NO+4H2O ���������ӣ���ֹ�������ӱ����� ��ȥ��������Sn2���� 2.5��10-5�� ����ϴ�ӹ�����FeSO4��7H2O����� 4:1:4:22
��������
��м����ϡ�����������������������������˺�õ���Һ������Һ����ϡ�����ữ����ͨ�����⣬������SnS��������ֹ�������ӱ����������˺�õ���ҺΪ����������������Ũ���ᡢ��ȴ�ᾧ�����˿ɵõ�FeSO4��7H2O
��1����ҵ�����ù���ϡ�����ܽ���м����������Ⱦ�����壬�䷴Ӧ���ӷ���ʽ�� 3Fe+8H�� +2NO3��=3Fe2�� +2NO+4H2O ���ʴ�Ϊ��3Fe+8H�� +2NO3��=3Fe2�� +2NO+4H2O��
��2���������̹�ϵͼ������ͨ�������Ʊ��ͣ�������ǿ��ԭ����Ŀ���dz��������ӣ���ֹ�������ӱ���������H2S������Һ�У�SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0�����������ϡ���������ҺPH=2Ϊ�˳�ȥ��������Sn2�����ʴ�Ϊ�����������ӣ���ֹ�������ӱ���������ȥ��������Sn2����
��3�� �����£�Ksp[Fe(OH)3]=4.0��10-38��Fe3��+3H2O Fe(OH)3+3H����Fe3+��ˮ�ⳣ��Ϊ
![]() =2.5��10-5���ʴ�Ϊ��2.5��10-5����
=2.5��10-5���ʴ�Ϊ��2.5��10-5����
��4������IV�õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ��ٳ�ȥ������渽�ŵ���������ʣ��ڱ�ˮ�¶ȵͣ������ܽ�ȼ�С������ϴȥ����������������ӣ������̷��ܽ��������ʧ���ʴ�Ϊ������ϴ�ӹ�����FeSO4��7H2O����ģ�
��5����һ����Ʒ��n(Fe2+)=![]() =0.03mol��n(Fe3+)=
=0.03mol��n(Fe3+)=![]() =0.04mol-0.03mol=0.01mol���ڶ�����Ʒn(SO42��)=
=0.04mol-0.03mol=0.01mol���ڶ�����Ʒn(SO42��)=![]() =0.04mol����������Ʒ��n(H2O)=
=0.04mol����������Ʒ��n(H2O)=![]() =0.225mol,���ݵ���غ㣺n(OH��)=0.01��3+0.03��2-0.04��2=0.01mol,�ᾧˮΪ0.225mol-0.01mol��
=0.225mol,���ݵ���غ㣺n(OH��)=0.01��3+0.03��2-0.04��2=0.01mol,�ᾧˮΪ0.225mol-0.01mol��![]() =0.22mol,x:y:z:w=(0.01+0.03):0.01:0.04:0.22=4:1:4:22��
=0.22mol,x:y:z:w=(0.01+0.03):0.01:0.04:0.22=4:1:4:22��
�ʴ�Ϊ��4:1:4:22��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2������һ��������������������������ˮ����������֪��NaClO2������Һ�ڵ���38��ʱ����NaClO23H2O������38��ʱ����NaClO2��
��1����ҵ�ϳ���ClO2�Ʊ���NaClO2�����Ա���������棬�������£�
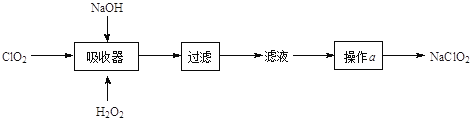
���������У�H2O2��������____���������������ԭ��������
������������ӦʱӦ�����¶ȵ���5���ԭ���ǣ�____��
�۲���a��55���������д�������������____���ý���38��~60�����ˮϴ�ӡ�����60�����õ�NaClO2���塣
��2����ClO2����ˮ�õ���Һ��Ϊ�ⶨ��Ũ�ȣ���������ʵ�������
����1��ȡ����ClO2��Һ20.00mL����ƿ�У�
����2����ϡH2SO4������ҺpH <2.0������������KI�����ַ�Ӧ��
����3�����뼸�ε�����Һ����μ���0.1 mol�� L-1��Na2S2O3��Һ��ǡ����ȫ��Ӧʱ������Na2S2O3��Һ20.00mL��
��֪��2ClO2+10KI+4H2SO4��2KCl+5I2+4K2SO4+4H2O��I2+2Na2S2O3��Na2S4O6+2NaI���Լ�����Һ��ClO2�����ʵ���Ũ�ȣ�д��������̣���____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Ҫ��Fe2O3��SiO2���Ʊ��̷���FeSO4��7H2O������ͨ���̷��Ʊ�����[FeO(OH)]���������£�����֪FeS2��������������ˮ��

��1���������������У���ò���___________________�����������������������������������ܽ�������
��2��д������ԭ�����跢����Ӧ�����ӷ���ʽ��___________________��
��3���ԡ���ԭ�������Һ����������X�����ɵõ��̷���������X����ָ___________________�����ˣ�ϴ�ӣ����
��4���벹���������顰��ԭ����������Һ���Ƿ���Fe3+��ʵ�鷽����ȡ����ԭ������Һ���Թ��ڣ�___________________��
��5�����һ���Ʊ������ķ�Ӧ�У�������һ�ֿ������ʵ����ʣ����Ļ�ѧʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������ͼװ�ý�����Ȫʵ�飬��֪Բ����ƿ�ڳ���X���壬��ͷ�ι���װ������YҺ�壬�ձ���װ������ZҺ�壬��������ܽ�����Ȫʵ��������Һ��һ���ܳ���������ƿ����
X���� | Y�Լ� | Z�Լ� | |
A | NO2 | H2O | H2O |
B | HCl | H2O | H2O |
C | HCl��O2������� | H2O | H2O |
D | NH3��N2������� | H2O | H2O |
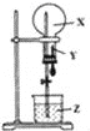
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ʵ���ҿ����Ʊ���������֤�������ʵ�װ��(���̶ֹ�װ����ʡ��)��
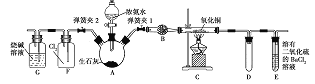
(1)���Ӻ�װ�ú���Ҫ���![]() װ�õ������ԣ���������ȹر�______��______����______����
װ�õ������ԣ���������ȹر�______��______����______����![]() ��װ��ˮ���þƾ�����
��װ��ˮ���þƾ�����![]() ���۲쵽
���۲쵽![]() �������ݲ������ƿ��ƾ��ƣ�
�������ݲ������ƿ��ƾ��ƣ�![]() �е�����ˮ���γɣ���˵��
�е�����ˮ���γɣ���˵��![]() װ�õ����������á�
װ�õ����������á�
(2)�����![]() ����ȡ������ԭ����_____________��
����ȡ������ԭ����_____________��
(3)װ��![]() ��ʢ�ŵ��Լ���______��
��ʢ�ŵ��Լ���______��
(4)�رյ��ɼ�2�����ɼ�1���ӷ�Һ©���зų�Ũ��ˮ����û��ƿ�е���ʯ�Һرշ�Һ©����������ȼ![]() ���ƾ��ƣ�װ��
���ƾ��ƣ�װ��![]() �кڰ�������죬װ��
�кڰ�������죬װ��![]() ��______(��ʵ������)����װ��
��______(��ʵ������)����װ��![]() ���ݳ����������ֱ�����˿����У���д��װ��
���ݳ����������ֱ�����˿����У���д��װ��![]() �з�����Ӧ�Ļ�ѧ����ʽ��____________��
�з�����Ӧ�Ļ�ѧ����ʽ��____________��
(5)��Ӧ�����رյ��ɼ�1�����ɼ�2�������������װ��![]() �У��ܿ췢��װ��
�У��ܿ췢��װ��![]() �в������̣�ͬʱ����װ��
�в������̣�ͬʱ����װ��![]() ����Һ������������װ��
����Һ������������װ��![]() �У�д��װ��
�У�д��װ��![]() �в������̵ķ�Ӧ�Ļ�ѧ����ʽ��______��װ��G����Һ����������ԭ����_______��
�в������̵ķ�Ӧ�Ļ�ѧ����ʽ��______��װ��G����Һ����������ԭ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2SO2(g)+O2(g)![]() 2SO3(g) ��H ����197kJ��mol��1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��1molO2��(��)1molSO2��0.5molO2��(��)2molSO3��1molO2�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ���ǣ� ��
2SO3(g) ��H ����197kJ��mol��1����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2molSO2��1molO2��(��)1molSO2��0.5molO2��(��)2molSO3��1molO2�����¡������·�Ӧ��ƽ��ʱ�����й�ϵһ����ȷ���ǣ� ��
A.������ѹǿP��P����P����2P��
B.����������ʵ���n��n����n����n��
C.SO3����������ӣ�����������������
D.��Ӧ��������ֵQ��197��Q����Q����Q��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ��������(KO2)����Ϊ����ɴ��յ���Դ��ijѧϰС���������ʵ��̽��KO2�����ʣ���ش�������⣺
I.̽��KO2��ˮ�ķ�Ӧ��ȡ����KO2�������Թ��У��μ�����ˮ���ٲ������ݣ��������ǵ�ľ�������Թܿ�ľ����ȼ���μӷ�̪��Һ���ȱ�����ɫ��
����ɫ����Һ�еμ�FeCl3��Һ�Ʋ����������Ϊ___��
II.̽��KO2��SO2�ķ�Ӧ
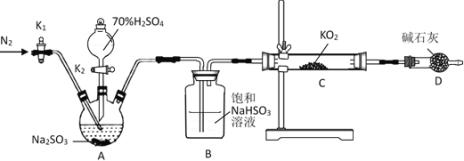
��1����ȷ�IJ���������__��
�ٴ�K1ͨ��N2 ���ž�װ����ԭ�����ر� �ڲ�жװ����ʵ�����
�ۼ��װ�������ԣ�Ȼ��װ��ҩƷ �ܴ�Һ©������K2
��2���������װ�������Եķ�����___��
��3��Aװ�÷����Ļ�ѧ����ʽΪ___��
��4��������װ����֤��KO2��SO2��Ӧ����O2�������ڲ��㣬��ĸĽ���ʩ��__��
��5���Ľ�����ʵ�飬��KO2��ȫ��Ӧ��װ��C�й����ˮ�ܽ⣬���50.00mL��Һ���ȷ�ΪM��N���ݡ�
����M��Һ�м��������������ữ��BaCl2��Һ����ַ�Ӧ���������ˡ�__��__������Ϊ2.33g��
�ڽ�N��Һ����__�����������ƣ��У���0.40mol/L����KMnO4��Һ�ζ����յ�ʱ��������KMnO4��Һ20.00mL��
������������������ݣ���д����ʵ���ܷ�Ӧ�Ļ�ѧ����ʽ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��CH4��Ϊ�����Ŀ�ȼ���塣
��1���������CO��CH4����ͬ�������·ֱ���ȫȼ�գ�ת�Ƶĵ�����֮��Ϊ___��
��2��120�棬101kPa�£�amL��CO��CH4��ɵĻ��������bmL��������ȫȼ�պָ���ԭ�����¶���ѹǿ��
�����������������ǡ����ȫ��Ӧ������bmLCO2������������CH4���������Ϊ__��
����ȼ�պ����������С��![]() mL����a��b��ϵ����ѧ����ʽΪ__��
mL����a��b��ϵ����ѧ����ʽΪ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ�~���ڱ��е�λ�ã��ش��������⣺

(1)�ؿ��к������ڵڶ�λ��Ԫ�������ڱ��е�λ����_______��
(2)�ڵ����������ķ���ʽΪ____��
(3)�١��ܡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����ۼ������ӻ����д������Ҫ���һ�ֻ�����ĵ���ʽ_____��
(4)W�ǵ����������ͬ�����Ԫ�ء��ݴ��Ʋ�W�����ܾ��е�������___
A.��������ϼ�Ϊ+6 B.��̬�⻯���H2S�ȶ�
C.����������Ӧˮ��������Ա������� D.�����ڳ����¿�����������
(5)��֪XΪ�ڢ�A��Ԫ��(��һ����������)����ԭ������Ϊa��Y��Xλ��ͬһ���ڣ���Ϊ�ڢ�A��Ԫ�أ���Y��ԭ������b��a���п��ܵĹ�ϵʽΪ____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com