
| 195×32.49% |
| 16 |
| 200×32.49% |
| 16 |
| 4×16 |
| 32.49% |
| 197×7.11% |
| 14 |
| 117 |
| 12 |
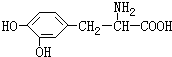 ,据此解答.
,据此解答.| 195×32.49% |
| 16 |
| 200×32.49% |
| 16 |
| 4×16 |
| 32.49% |
| 197×7.11% |
| 14 |
| 117 |
| 12 |
 ,
, ,含有的官能团的名称是:羧基、酚羟基、氨基,故答案为:197g/mol;
,含有的官能团的名称是:羧基、酚羟基、氨基,故答案为:197g/mol;  ;羧基、酚羟基、氨基;
;羧基、酚羟基、氨基;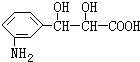 等,故答案为:
等,故答案为: 等;
等;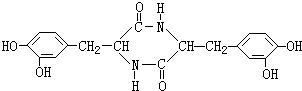 ,
, .
.


科目:高中化学 来源: 题型:
| A、标准状况下,22.4L水中含有的氧原子数为NA |
| B、0.3molNO2与水反应时转移的电子数为0.2NA |
| C、标准状况下,28gN2和CO所组成的混合气体,其体积为22.4L |
| D、足量铁粉与1molCl2在加热条件下充分反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
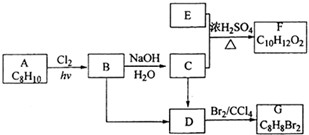
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
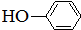 合成
合成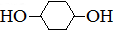 .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)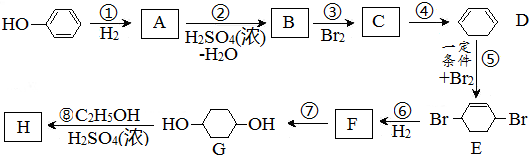
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定只有C、H、O |
| B、可能含有C、H、O |
| C、一定含有C、H、无O |
| D、一定含有C、H、可能有O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种难溶物质比较,溶度积小的溶解度不一定小 | ||||
| B、水的离子积常数KW随着温度的升高而增大,说明水的电离是放热反应 | ||||
C、向0.1mol/L的氨水中加入少量硫硫酸固体,则溶液中
| ||||
| D、0.1mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 | B、3 | C、5 | D、6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com