
| A. | 根据纯净物的元素组成,将纯净物分为单质和化合物 | |
| B. | 根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等 | |
| C. | 根据能水溶液能否电离出氢离子,来判断化合物是否是酸 | |
| D. | 根据是否含金属元素,来判断氧化物是否是碱性氧化物 |
分析 A.一种物质组成的为纯净物,同种元素组成的纯净物为单质,不同元素组成的纯净物为化合物;
B.水溶液中能电离出的氢离子显酸性;
C.水溶液中电离出的阳离子全部是氢离子的化合物;
D.和酸反应生成盐和水的氧化物为碱性氧化物.
解答 解:A.根据纯净物的元素组成,同种元素组成的纯净物为单质,不同元素组成的纯净物为化合物,将纯净物分为单质和化合物,故A正确;
B.根据酸分子中含有能电离的氢原子个数将酸分为一元酸、二元酸等,故B错误;
C.水溶液中电离出的阳离子全部是氢离子的化合物为酸,故C错误;
D.含金属元素的氧化物可能为两性氧化物如Al2O3,酸性氧化物Mn2O7,故D错误;
故选A.
点评 本题考查了物质分类、物质组成、酸碱概念的分析,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2NO2 (g)?N2O4(g)△H<0 | B. | C(s)+CO2 (g)?2CO(g)△H>0 | ||
| C. | N2(g)+3H2 (g)?2NH3(g)△H<0 | D. | H2S (g)?H2 (g)+S(s)△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液 | |
| B. | 配制一定物质的量浓度的稀盐酸时,用量筒量取9.82 mL浓盐酸 | |
| C. | 配制1 L 0.1 mol•L-1的NaCl溶液时用托盘天平称量5.85 g NaCl固体 | |
| D. | 定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | p(N2)>p(H2)>p(O2) | B. | p(O2)>p(N2)>p(H2) | C. | p(N2)>p(O2)>p(H2) | D. | p(H2)>p(N2)>p(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
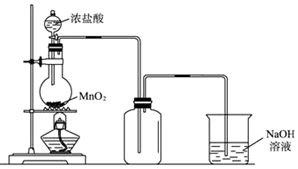
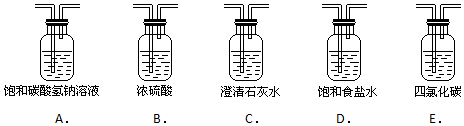
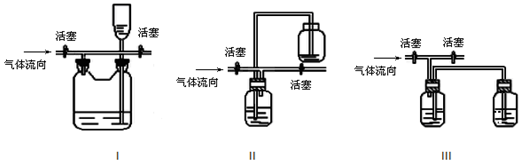
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
下列物质的水溶液能导电,但属于非电解质的是
A.Na2S B. Cl2 C. NaHCO3 D. CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com