
���б�ʾ��ѧ���̵Ļ�ѧʽ��д��ȷ���ǣ�
A������������Һ�Լ��ԣ�SO32��+2 H2O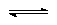 H2SO3 +2 OH��
H2SO3 +2 OH��
B���Ȼ���Ͷ��ˮ�к���ƽ�⣺AgCl (s) Ag+ (aq) + Cl��(aq)
Ag+ (aq) + Cl��(aq)
C�������ȼ����Ϊ890.3kJ��mol-1����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ��
CH4(g)+2O2(g)��CO2(g)+2H2O(g) ��H=��890.3kJ��mol-1
D��500�桢30MPa�£���0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3kJ���Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)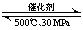 2NH3(g) ��H=��38.6 kJ��mol-1
2NH3(g) ��H=��38.6 kJ��mol-1

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���еݱ�����У���ȷ����( )
A. Na��Mg��Alԭ�ӵ��������������μ���
B. Si��P��SԪ�ص�����������ν���
C. C��N��O��ԭ�Ӱ뾶���μ�С
D. Li��Na��K�Ľ��������μ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�����Һ�У�c( )�����ǣ� ��
)�����ǣ� ��
A��250 mL 1 mol��LFeCl3 B��800 mL 0.5 mol��L MgCl2
C��500 mL 1 mol��L KCl D��200 mL 1 mol��LCaCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��8���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�������ʾ��ͼһ�µ��ǣ� ��
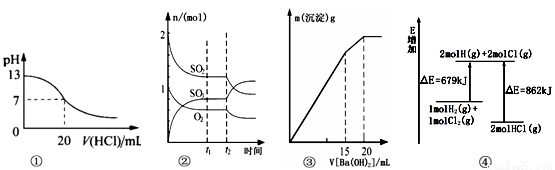
A��ͼ�ٱ�ʾ25��ʱ����0��1 mol/L����ζ�20 mL 0��1 mol/L NaOH��Һ����Һ��pH�����������ı仯�õ��ĵζ�����
B��ͼ�ڱ�ʾһ�������½��еķ�Ӧ2SO2(g) + O2(g) 2SO3(g) ��H < 0���ɷֵ����ʵ����仯��t2ʱ�̸ı�����������ǽ����¶Ȼ���С�������
2SO3(g) ��H < 0���ɷֵ����ʵ����仯��t2ʱ�̸ı�����������ǽ����¶Ȼ���С�������
C��ͼ�۱�ʾij������Һ�м���Ba(OH)2��Һ�����������������Ba(OH��Һ����Ĺ�ϵ���ڼ���20 mL Ba(OH)2��Һʱ������ǡ�ó�����ȫ
D��ͼ�ܱ�ʾ��ѧ��ӦH2(g)+C12(g)== 2HCl(g)�������仯����÷�Ӧ�ķ�Ӧ�ȡ�H=��183 kJ��mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��8���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�������ӷ�Ӧ������������ԭ��Ӧ����
A��Fe + CuSO4 = Cu + FeSO4 B��2Na + Cl2  2 NaCl
2 NaCl
C��NaCl + AgNO3 = AgCl��+ NaNO3 D��2KClO3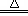 2KCl + 3O2��
2KCl + 3O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��8���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���ͬ���ʵ���Ũ�ȵ��������ʵ���Һ����PH��С��˳�����е�Ϊ
A��NaHSO4 CH3COONa NH4Cl NaNO3
B��NaNO3 CH3COONa NaHSO4 NH4Cl
C��NaNO3 CH3COONa NH4Cl NaHSO4
D��CH3COONa NaNO3 NH4Cl NaHSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��8���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ճ������Լ����������Ź㷺�����á����й��ڽ�����һЩ˵������ȷ����
A���Ͻ����������ɷֽ��������ʲ���ȫ��ͬ
B����ҵ�Ͻ���Mg��Al�����õ�����ڵ��Ȼ����Ƶõ�
C������ұ���ı����ǽ��������ӵõ����ӱ�ɽ���ԭ��
D��Խ���õĽ���Խ��ұ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������и�����ѧ�ڿ�ѧ�⻯ѧ�Ծ��������棩 ���ͣ������
��1����100 mL 0.8mol/L������Һ�м�������ͭ�ۣ����ܽ��ͭ������Ϊ____________g��
��2����������Һ���ټ�������ϡ���ᣬ����_______gͭ�ܽ⡣�˹��������ɵ������ڱ�״���µ����Ϊ_________L��
��3������100 mL 0.8mol/L������Һ�м������ۣ���÷�Ӧ�����Һ��Fe2+��Fe3+��Ũ��֮��Ϊ1:1���������������Ϊ____________g��
��4����100 mL 0.8mol/L������Һ�м���һ����Fe��FeO��Fe2O3�Ļ�����ַ�Ӧ�ų�����224mL(��״����)���Ҳ����Һ����Ԫ��ֻ��Fe2+��ʽ���ڣ�ΪʹFe2+��ȫ����������Ӧ�����Һ�м���0.1mol/L��NaOH��Һ___________mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡɳ�и�����ѧ�ڵ����ο��Ի�ѧ�Ծ��������棩 ���ͣ������
��ҵ������������ʱ����ͬʱ������һ�ֳ�������Ҫ������������Ư����������(NaClO2)���乤���������£�
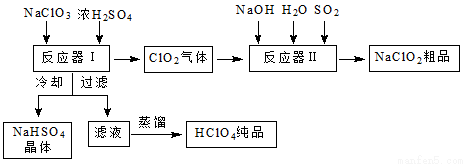
��֪����NaHSO4�ܽ�����¶ȵ����߶������ʵ������¿ɽᾧ������
�ڸ�����������Ϊֹ������֪���е���ǿ�ᣬ�е�90 �档
��ش��������⣺
��1����Ӧ�����з�����Ӧ�Ļ�ѧ����ʽΪ ����ȴ��Ŀ���� ��������������������ԭ����___________________��
��2����Ӧ�����з�����Ӧ�����ӷ���ʽΪ__________________________��
��3��ͨ�뷴Ӧ�����е�SO2��H2O2����ͬ��������NaClO2�����Ҫ˵��˫��ˮ�ڷ�Ӧ���ܴ���SO2��ԭ����___________________��
��4�� Ca(ClO)2��ClO2��NaClO2�Ⱥ��Ȼ����ﶼ�dz��õ���������Ư��������Ϊ���Ƕ�����__________����д����ҵ������������ʯ������Ư�۾��Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com