
��������A��ʾ��ƽ����Ӧ����Ϊ0.3 mol��L-1��s-1 ��������B��ʾ��ƽ����Ӧ����Ϊ0.6 mol��L-1��s-1 ��2 sʱ����A��ת����Ϊ70% ��2 sʱ����B��Ũ��Ϊ0.7 mol��L-1
A.�٢� B.�٢� C.�ڢ� D.�ۢ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A.�٢� B.�٢� C.�ڢ� D.�ۢ�?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꽭��ʡ������ѧ�߶���ѧ����ĩ���Ի�ѧ���⣨ѡ�ޣ� ���ͣ���ѡ��
�� 4 mol A ����� 2 mol B ������ 2 L �Ķ��������л�ϲ���һ�������·������·�Ӧ �� ���� 2 s���� C �����ʵ���Ũ��Ϊ 0.6 mol��L-1���������м���˵����
���� 2 s���� C �����ʵ���Ũ��Ϊ 0.6 mol��L-1���������м���˵����
�� ������ A ��ʾ�����ʱ���ƽ������Ϊ 0.3 mol��L-1��s-1
�� ������ B ��ʾ�����ʱ���ƽ������Ϊ 0.6 mol��L-1��s-1
�� 2 s ʱ���� A ��ת����Ϊ30%
�� 2 s ʱ���� B �����ʵ���Ũ��Ϊ 0.3mol��L-1
������ȷ����
| A���٢� | B���ڢ� | C���٢� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
�� 4 mol A ����� 2 mol B ������ 2 L �������л�ϲ���һ�������·������·�Ӧ��2A��g����B��g��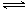 2C��g��,���� 2 s���룩����C ��Ũ��Ϊ 0.6 mol��L��1 ����
������ A ��ʾ�ķ�Ӧ��ƽ������
�� 2 s ʱ���� B ��Ũ��Ϊ
��
2C��g��,���� 2 s���룩����C ��Ũ��Ϊ 0.6 mol��L��1 ����
������ A ��ʾ�ķ�Ӧ��ƽ������
�� 2 s ʱ���� B ��Ũ��Ϊ
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��4 mol A�����2 mol B������2L �������л�ϲ���һ�������·������·�Ӧ��2A(g)+B(g)
 2C(g)����2s ����C��Ũ��Ϊ0.6mol•L-1�������м���˵�����в���ȷ����
2C(g)����2s ����C��Ũ��Ϊ0.6mol•L-1�������м���˵�����в���ȷ����
A. ������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3 mol•L-1•s-1
B. 2sʱ��ѹǿ����ʼʱ��1.1��
C. 2sʱ����A��ת����Ϊ30%
D. 2sʱ����B��Ũ��Ϊ0.7 mol•L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�츣��ʡ�ĵ���У��һ��ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��4 mol A �����2 mol B ������2 L�������л�ϲ���һ�������·������·�Ӧ��
2A��g��+B��g��  2C��g������2 s ����C��Ũ��Ϊ0.6 mol/L�����м���˵����ȷ����
2C��g������2 s ����C��Ũ��Ϊ0.6 mol/L�����м���˵����ȷ����
��������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3 mol/��L��s��
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol/��L��s��
�۷�Ӧ�ﵽƽ��ʱ��A��B��C�ķ�Ӧ����һ�����
�ܷ�Ӧ�ﵽƽ��ʱ��A��B��C�����ʵ��������ٱ仯
A���٢� B���٢� C���ڢ� D���ۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com