
| A. | ①②③ | B. | 只有②③④ | C. | ②③④⑤ | D. | 全部都行 |
分析 二氧化硫既有氧化性又有还原性,而二氧化碳在溶液中不发生氧化还原反应,且二氧化硫具有漂白性,二者均为酸性氧化物,都能使石灰水变浑浊,以此来解答.
解答 解:①SO2和CO2都属于酸性氧化物,它们都能使澄清石灰水变浑浊,所以不能利用澄清石灰水来区别SO2和CO2;
②SO2具有氧化性,能将H2S溶液氧化生成单质(有黄色沉淀生成),而CO2没有此性质,所以能利用H2S溶液区别SO2和CO2;
③SO2具有还原性,能被KMnO4酸性溶液氧化(溶液褪色),而CO2没有此性质,所以能利用KMnO4酸性溶液区别SO2和CO2;
④SO2具有还原性,能被氯水氧化(溶液褪色),而CO2没有此性质,所以能利用氯水区别SO2和CO2;
⑤SO2具有漂白性,能使品红溶液褪色,而CO2没有此性质,所以能利用品红溶液区别SO2和CO2;
所以能够区别SO2和CO2气体的溶液有:②③④⑤,
故选C.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意二氧化硫的还原性及漂白性,题目难度不大.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:解答题
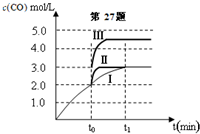 甲醇是重要的化学工业基础原料和清洁液体燃料.工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
甲醇是重要的化学工业基础原料和清洁液体燃料.工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O (g) | K3 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液 | |
| B. | 10 g46%的乙醇水溶液中所含氢原子数目为1.2NA | |
| C. | 200 ml1mol/LFe2(SO4 )3溶液中,Fe3+和SO42-离子数的总和是NA | |
| D. | 可用电解氯化镁溶液的方法制取金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 所示.
所示. 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下:
 .
. .
. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 今年两会的一个主题是环境保护,治理雾霾天气是我们目前最主要的一个任务.如图是北京统计的雾霾天气的来源和成分分析:下列对于治理雾霾天气措施描述不正确的是( )
今年两会的一个主题是环境保护,治理雾霾天气是我们目前最主要的一个任务.如图是北京统计的雾霾天气的来源和成分分析:下列对于治理雾霾天气措施描述不正确的是( )| A. | 充分的洗涤燃煤,除去燃煤表面的灰尘 | |
| B. | 加快我国由“燃煤”时代进入到“油气”时代的步伐 | |
| C. | 采用催化转换技术将汽车尾气中的NO2和CO转化为无毒气体 | |
| D. | 处理NO2的一种方法是利用甲烷催化还原NO2,若CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-512kJ•mol-1,则1g甲烷处理NO2需要放出16kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烯、聚乙烯、苯乙炔都是不饱和烃 | |
| B. | 苯能与溴水在一定条件下发生取代反应 | |
| C. | 减少化石燃料使用,有利于降低空气中PM2.5(直径2.5μm以下细颗粒物)的含量 | |
| D. | 乙烯、苯、甲苯都能使高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| C. | 由氯代环己烷消去制环己烯;由乙醇制乙烯 | |
| D. | 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两粒子的1s能级上电子的能量相同 | |
| B. | 两粒子的3p能级上的电子离核的距离相同 | |
| C. | 两粒子都达8电子稳定结构,化学性质相同 | |
| D. | 两粒子的电子发生跃迁时,产生的光谱不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com