
| A.把石油经蒸馏分离成为汽油,煤油和柴油等 |
| B.煎中药时用水在煮沸条件下提取中药的有效成分 |
| C.把大豆磨碎后,用水溶解其中的可溶性成分,经过滤后,分成豆浆和豆渣 |
| D.做饭洗米时淘去米中的沙 |
科目:高中化学 来源:不详 题型:单选题
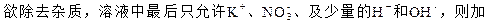 入试剂的顺序正确的是
入试剂的顺序正确的是 | A.Ba(NO3)2K2CO3KOH AgNO3HNO3 |
| B.AgNO3KOH K2CO3Ba(NO3)2HNO3 |
| C.KOH AgNO3Ba(NO3)2K2CO3HNO3 |
| D.KOH Ba(NO3)2K2CO3AgNO3HNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
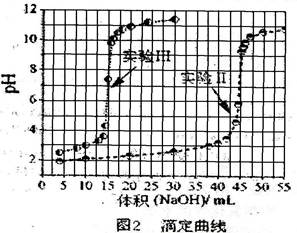 实验I 从第一瓶溶液中取出25.00 mL,以标准NaOH溶液滴定,滴定结果列于表1中。
实验I 从第一瓶溶液中取出25.00 mL,以标准NaOH溶液滴定,滴定结果列于表1中。| 体积(NaOH)/mL | pH | ||
| 5.0 | 2.2 | ||
| 10.0 | 2.4 | ||
| 3.0 | ||
| 24.0 | 3.8 | ||
| 24.8 | 4.5 | ||
| 25.0 | 7.0 | ||
| 25.2 | 9.5 | ||
| 26.0 | 10.0 | ||
| 30.0 | 10.7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来 |
| B.水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热的蒸馏法使含水酒精变为无水酒精 |
| C.可用冷却热的饱和氯化钾和氯化钠的溶液的方法得到纯净的氯化钠晶体 |
| D.由于胶体微粒的粒度比离子大,所以碘化钾混入淀粉中可用渗析法分离 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
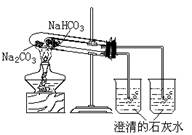
| A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢 |
| B.分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少 |
| C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成 |
| D.分别将等量的白色粉末用右图装置进行实验,比较澄清石灰水是否变混浊 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH | B.盐酸 | C.酚酞试液 | D.BaCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
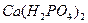 ,有人拟用
,有人拟用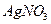 、
、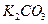 、KOH和
、KOH和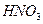 作试剂除去杂质,且最后溶液中只含
作试剂除去杂质,且最后溶液中只含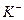 、
、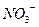 、
、 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

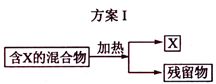
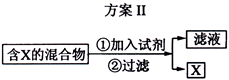
 (1)选用方案I时,X应该具有的性质是 ,残留物应该具有的性质是 ;
(1)选用方案I时,X应该具有的性质是 ,残留物应该具有的性质是 ; (2)选用方案Ⅱ从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是 ,有关反应的化学方程式为 ;
(2)选用方案Ⅱ从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是 ,有关反应的化学方程式为 ; (3)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),参照方案I和Ⅱ,请设计一种以框图形式表示的实验方案(注明物质和操作) 。
(3)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),参照方案I和Ⅱ,请设计一种以框图形式表示的实验方案(注明物质和操作) 。查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
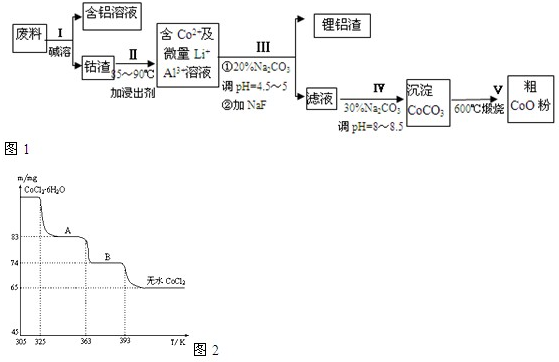
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com