
【题目】某学习小组用碳素钢进行了以下探究活动:
(1)[探究一]将已去除表面氧化膜的碳素钢钉放入冷浓硫酸中,10min后将钢钉浸入CuSO4溶液中,钢钉表面无明显变化,其原因是
(2)称取6.0g碳素钢放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y.①甲同学认为X中除Fe3+之外还可能含有Fe2+ , 若要确认是否含有Fe2+ , 可选用(选填序号).
A.KSCN溶液 B.浓氨水 C.酸性KMnO4溶液 D.K3[Fe(CN)6]溶液
②乙同学取560mL(标准状况)干燥气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g,由此可知Y中含硫化合物Q1的体积分数为 .
[探究二]丙同学认为气体Y中还可能含有Q2、Q3两种气体(相同条件下Q1、Q2、Q3气体的密度依次减小).为此,设计了下列装置进行实验探究(假设有关气体完全反应).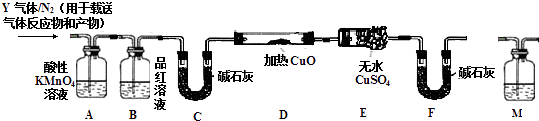
(3)装置B中试剂的作用是 .
(4)已知洗气瓶M中盛装的是澄清石灰水,为确认Q2的存在,洗气瓶M的位置应在 , 产生Q2的反应的化学方程式为 .
(5)确认含有气体Q3的实验现象是 , 产生Q3的反应的离子方程式为 .
【答案】
(1)Fe表面被浓硫酸作用发生了钝化,生成了一层氧化物膜
(2)CD;80%
(3)确认SO2已除尽
(4)B与C之间;C+2H2SO4(浓) ![]() ?CO2↑+2SO2↑+2H2O
?CO2↑+2SO2↑+2H2O
(5)D中固体由黑变红、E中固体由白变蓝;Fe+2H+═Fe2++H2↑
【解析】解:[探究一](1)常温下,Fe易和浓硫酸发生氧化还原反应生成致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以放入浓硫酸后的碳素钢加入硫酸铜溶液中无变化,说明Fe表面发生了钝化,生成了一层氧化物膜,所以答案是:Fe表面被浓硫酸作用发生了钝化,生成了一层氧化物膜;(2)①亚铁离子具有还原性,而酸性高锰酸钾有氧化性,发生氧化还原反应使高锰酸钾溶液褪色,亚铁离子遇到K3[Fe(CN)6]溶液变蓝色,故选CD,所以答案是:CD;②SO2+Br2+2H2O=2HBr+H2SO4 , H2SO4+BaCl2=BaSO4↓+2HCl,所以硫酸钡和二氧化硫之间的关系式为SO2﹣﹣﹣﹣﹣BaSO4 , 设二氧化硫的体积为V,SO2﹣﹣﹣﹣﹣BaSO4 ,
22.4L 233g
V 4.66g
V=0.448l=448mL,
所以二氧化硫的体积分数= ![]() ×100%=80%,所以答案是:80%;[探究二]称取6.0g碳素钢放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y,气体Y中还可能含有Q2、Q3两种气体(相同条件下Q1、Q2、Q3气体的密度依次减小)依据反应实质分析可知,浓硫酸和铁反应生成硫酸铁、二氧化硫和水,所含碳和浓硫酸加热反应生成二氧化碳、二氧化硫和水,随反应进行浓硫酸变为稀硫酸和铁反应生成气体为氢气,Q1、Q2、Q3气体成分为SO2、CO2、H2 , 依据装置通过装置A中高锰酸钾溶液除去二氧化硫,装置B中品红溶液检验二氧化硫是否除净,通过碱石灰吸收二氧化碳、水蒸气,通过装置D加热的氧化铜和氢气发生反应生成铜和水蒸气,进入装置F无水硫酸铜变蓝色,装置F是防止空气中水蒸气进入装置F影响产物检验,(3)二氧化硫能使品红溶液褪色,所以用品红溶液检验二氧化硫是否除尽,所以答案是:确认二氧化硫已经除尽;(4)二氧化硫和二氧化碳都能使澄清石灰水变浑浊,但二氧化硫还能使品红溶液褪色,所以要检验二氧化碳必须排除二氧化硫的干扰,B装置是检验二氧化硫是否除尽,所以澄清石灰水应放置在B和C之间,碳素钢中含有碳,加热条件下,碳能和浓硫酸反应生成二氧化硫、二氧化碳和水,反应方程式为:C+2H2SO4(浓)
×100%=80%,所以答案是:80%;[探究二]称取6.0g碳素钢放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y,气体Y中还可能含有Q2、Q3两种气体(相同条件下Q1、Q2、Q3气体的密度依次减小)依据反应实质分析可知,浓硫酸和铁反应生成硫酸铁、二氧化硫和水,所含碳和浓硫酸加热反应生成二氧化碳、二氧化硫和水,随反应进行浓硫酸变为稀硫酸和铁反应生成气体为氢气,Q1、Q2、Q3气体成分为SO2、CO2、H2 , 依据装置通过装置A中高锰酸钾溶液除去二氧化硫,装置B中品红溶液检验二氧化硫是否除净,通过碱石灰吸收二氧化碳、水蒸气,通过装置D加热的氧化铜和氢气发生反应生成铜和水蒸气,进入装置F无水硫酸铜变蓝色,装置F是防止空气中水蒸气进入装置F影响产物检验,(3)二氧化硫能使品红溶液褪色,所以用品红溶液检验二氧化硫是否除尽,所以答案是:确认二氧化硫已经除尽;(4)二氧化硫和二氧化碳都能使澄清石灰水变浑浊,但二氧化硫还能使品红溶液褪色,所以要检验二氧化碳必须排除二氧化硫的干扰,B装置是检验二氧化硫是否除尽,所以澄清石灰水应放置在B和C之间,碳素钢中含有碳,加热条件下,碳能和浓硫酸反应生成二氧化硫、二氧化碳和水,反应方程式为:C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O,所以答案是:B与C之间,C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,所以答案是:B与C之间,C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O;(5)确认含有气体Q3为氢气的实验现象是,氢气还原氧化铜固体黑色变化为红色,生成气体中含水蒸气,遇到无水硫酸铜变蓝色,确认含有气体Q3的实验现象是D中固体由黑变红、E中固体由白变蓝,产生Q3的反应的离子方程式为Fe+2H+═Fe2++H2↑,所以答案是:D中固体由黑变红、E中固体由白变蓝,Fe+2H+═Fe2++H2↑;
CO2↑+2SO2↑+2H2O;(5)确认含有气体Q3为氢气的实验现象是,氢气还原氧化铜固体黑色变化为红色,生成气体中含水蒸气,遇到无水硫酸铜变蓝色,确认含有气体Q3的实验现象是D中固体由黑变红、E中固体由白变蓝,产生Q3的反应的离子方程式为Fe+2H+═Fe2++H2↑,所以答案是:D中固体由黑变红、E中固体由白变蓝,Fe+2H+═Fe2++H2↑;


 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短元素在元素周期表中的相对位置如图所示,其中X、W的质子数之和为22,由此可知
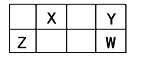
A. X位于元素周期表中第2周期,第VA族
B. Y的氢化物(H2Y)不稳定,100℃以上即可分解
C. Z的最高价氧化物的水化物是一种强碱
D. W的非金属性比X的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个体积相同的密闭容器中分别充入NH3、CO2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是
A. p(NH3)>p(CO2)>p(O2)B. p(NH3)> p(O2)> p(CO2)
C. p(CO2)> p(O2)> p(NH3)D. p(CO2)> p(NH3)> p(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
A. 空气、硫酸铜、硫酸B. 水、空气、纯碱
C. 氧化铁、胆矾、熟石灰D. 硝酸、食盐水、烧碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】良好的生态环境可以提升生活质量.
①近几年来,我国多次出现大范围雾霾天气,许多城市发布PM2.5重度污染警报.下列行为能缓解城市大气中PM2.5浓度的是(填字母).
a.燃放烟花爆竹 b.为城市主干道洒水保洁 c.大面积开发土建项目
②垃圾无害化处理有利于保护生态环境.下列有关生活垃圾的处理合理的是
(填字母).
a.废旧塑料露天焚烧 b.用厨房垃圾生产沼气 c.废旧电池就地填埋
③选择环保的装修材料可以有效地减少居室污染.劣质胶合板释放的主要污染物是(填字母).
a.NO b.CO c.甲醛
④光化学烟雾主要是氮氧化物所造成的.工业上可用氨气在催化剂作用下与之反应生成对空气无污染的物质.请写出氨气与二氧化氮反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PAFC{聚合碱式氯化铝铁,通式:[FeaAlb(OH)xCly]n}是一种新型的无机高分子絮凝剂.以高铁铝土矿、硫酸厂渣尘为配料(主要成分:Al2O3、Fe2O3 , 杂质FeO、SiO2等)为原料制取PAFC的实验流程如下: 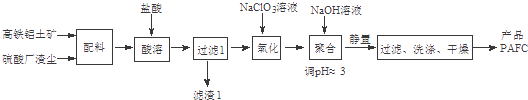
(1)为提高“酸溶”速率,除适当增大盐酸浓度外,还可采取的措施有(举一例).
(2)“酸溶”时,Al2O3与盐酸反应的化学方程式为 , 滤渣1的主要成分为(写化学式)
(3)“氧化”时,NaClO3氧化Fe2+ , 本身被还原为Cl﹣ , 该反应的离子方程式为 .
(4)“聚合”时,若将溶液pH调得过高,可能造成的影响是 .
(5)![]() 是衡量PAFC净水效果的重要参数之一,某合作学习小组的同学拟通过实验确定产品中
是衡量PAFC净水效果的重要参数之一,某合作学习小组的同学拟通过实验确定产品中 ![]() 的比值. 步骤1.准确称取5.710g样品,溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到3.350g固体.
的比值. 步骤1.准确称取5.710g样品,溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到3.350g固体.
步骤2.另准确称取2.855g样品,溶于足量NaOH溶液,过滤,充分洗涤,将滤渣灼烧至质量不再变化,得到固体0.4000g.
①通式[FeaAlb(OH)xCly]n中,a、b、x、y的代数关系式为
②产品中n(Al)/n(Fe)的比值为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中前者为电解质、后者属于非电解质的是
A.CaO、C2H5OH B.HCl、CH3COOH C.H2S、 BaSO4 D.NH3·H2O、Cu
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com