
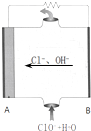
 镁燃料电池具有高比能量、安全和成本低等特点,在军事和民用方面有良好的应用前景.镁燃料电池的氧化剂可以利用空气或者海水中的氧,还有过氧化氢和次氯酸盐等.
镁燃料电池具有高比能量、安全和成本低等特点,在军事和民用方面有良好的应用前景.镁燃料电池的氧化剂可以利用空气或者海水中的氧,还有过氧化氢和次氯酸盐等.

科目:高中化学 来源: 题型:
| A、原子半径:A<B<C |
| B、A的氢化物稳定性小于C的氢化物稳定性 |
| C、三种元素的最高价氧化物对应的水化物均可由化合反应得到 |
| D、高温下,B单质能置换出A单质,A单质能置换出C单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上在合成塔中采用下列反应合成甲醇:
工业上在合成塔中采用下列反应合成甲醇:| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡 时数 据 | CH3OH的浓度(mol?L-1) | c1 | c2 | c3 |
| 反应吸收或放出的能量(KJ) | a | b | c | |
| 体系压强(Pa) | P1 | P2 | P3 | |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E、F六种物质有如下转化关系(部分生成物已略去).已知A、C、F均为钠盐,其中固体C受热分解可生成固体F、气体B和水,气体单质E的相对分子质量比B大27.请回答下列问题:
A、B、C、D、E、F六种物质有如下转化关系(部分生成物已略去).已知A、C、F均为钠盐,其中固体C受热分解可生成固体F、气体B和水,气体单质E的相对分子质量比B大27.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容器中总压强不随时间变化而变化 |
| B、单位时间内断裂一个A-A键,同时生成两个C-C键 |
| C、v正(B)=0.03mol/(L?s),v逆(D)=1.2mol/(L?min) |
| D、容器中气体的平均相对分子质量不随时间变化而变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com