
【题目】用无机矿物资源生产部分材料,其生产流程如图.下列有关说法不正确的是( ) 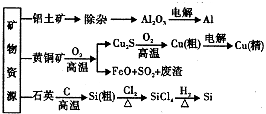
A.Al2O3、SiCl4均为共价化合物
B.生产过程中均涉及氧化还原反应
C.石英可用于制光导纤维,晶体Si常用做半导体材料
D.黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用于冶炼铁
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】检验溴乙烷中是否有溴元素,主要的实验方法是( )
A.加入氯水后振荡,看水层里是否有棕红色的溴出现
B.加入硝酸银溶液,再加稀硝酸,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,冷却后加硝酸银溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,冷却后用过量稀硝酸中和过量的碱后,再加硝酸银溶液,观察有无浅黄色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1molL﹣1氢氧化钠溶液与0.06molL﹣1硫酸溶液等体积混合,该混合溶液的pH等于( )lg2=0.3.
A.1.7
B.2.0
C.12.0
D.11.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的分子式为C10H14 , 它不能使溴水褪色,但可使KMnO4酸性溶液褪色,分子结构中只含有一个烷基,符合条件的烃有( )
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纳米材料氧缺位铁酸盐(MFe2Ox)(32、NO2等氧化物转化为单质。转化流程如图所示,下列有关该转化过程的叙述不正确的是
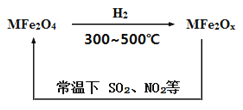
A. MFe2O4表现了氧化性
B. 若MFe2Ox与SO2发生反应的物质的量之比为3:1,则x=10/3
C. 在处理该废气过程中,每处理含1moINO2的废气转移电子数4NA个
D. MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)2SO2(g)+O2(g) △ v 2 O 5 2SO3(g);△H=﹣196.6KJ/mol,是制备硫酸的重要反应.下列关于该反应的叙述正确的是 . (填字母)
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1 , c2 , 则时间间隔t1~t2内,SO3(g)生成的平均速率为u= c 2 c 1 t 2 t 1
E.使用催化剂V2O5能提高SO2的转化率
F.使用催化剂V2O5会改变该反应的△H
(2)判断该反应达到平衡状态的标志是 .(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.在体积不变的容器中,气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.在体积不变的容器中混合气体,的密度保持不变
f.SO2、O2、SO3的浓度比保持不变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式错误的是( )
A.用硅酸钠与盐酸反应制备硅胶:SiO ![]() +2H+═H2SiO3(胶体)
+2H+═H2SiO3(胶体)
B.FeI2溶液中通入少量Cl2:2Fe2++Cl2═2Fe3++2Cl﹣
C.少量NaHSO4 溶液与Ba(OH)2 溶液反应:H++OH﹣+SO ![]() +Ba2+═H2O+BaSO4↓
+Ba2+═H2O+BaSO4↓
D.FeCl3溶液中通入SO2 , 溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO ![]() +4H+
+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体5.6L(标准状况),同时溶液质量增加9.3g,下列判断正确的是( )
A.原溶液中投入铁粉物质的量是0.25mol
B.原溶液中的HNO3浓度是2.0mol/L
C.反应后的溶液中还可以溶解9.6g铜
D.反应后的溶液中c(Fe2+):c(Fe3+)=1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com