
| ① | He-268.8 | Ne-249.5 | Ar(x) | Kr-151.7 |
| ② | F2-187.0 | Cl2-33.6 | (a)58.7 | I2-184.0 |
| ③ | HF(Y) | HCl-84.0 | HBr-67.0 | HI-35.3 |
| ④ | H2O(Z) | H2S-60.2 | (b)-42.0 | H2Te-1.8 |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
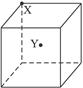
| A.若X是原子晶体,Y是分子晶体,则熔点:X<Y |
| B.若A2+2D-===2A-+D2,则氧化性:D2>A2 |
| C.若R2-和M+的电子层数相同,则原子序数:R>M |
| D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.PCl5中所有的原子都满足最外层8电子结构 |
| B.同素异形体之间的转化属于物理变化 |
| C.质子数相等,电子数也相等的良种微粒可能是不同的离子 |
| D.CaF2和Na2O2的化学键和晶体类型均相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
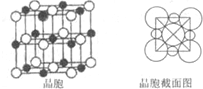
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
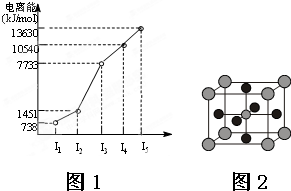
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙醇蒸汽通过灼热的CuO粉末 | B.二氧化碳通过Na2O2粉末 |
| C.铝与Fe2O3发生铝热反应 | D.将锌粒投入Cu(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品 |
| B.NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂 |
| C.NH3能与Cl2生成NH4Cl,可用浓氨水检验输送氯气的管道是否有泄漏 |
| D.K2FeO4能与水作用生成Fe(OH) 3胶体和O2,可用于自来水的净化和杀菌消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com