
����Ŀ�����ԭ����ԭ���ԭ���ǵ绯ѧ��������Ҫ���ݡ�ij��ȤС��������̽��ʵ�飺
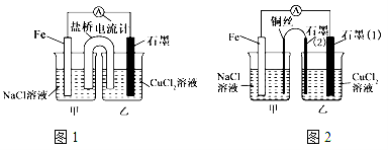
��1������ͼ1Ϊijʵ��С������������ԭ��Ӧ��Ƶ�ԭ���װ�ã���������װ�б��͵�KNO3��Һ�������ƳɵĽ���,��NO3-����_____________װ������д�����ҡ����������������䣬����CuCl2��Һ��ΪNH4Cl��Һ������������ɫ��ζ�ĵ������壬��ʯī�ϵ缫��Ӧʽ______________________��
��2������ͼ2�������������䣬�������Ż�����ͭ������ʯī������n�ͣ����װ����____________���ԭ��ػ���ء�������װ����ʯī��2��Ϊ ������װ����������������ʯī��1���缫�Ϸ����ķ�ӦʽΪ ��
��3����ͼ2��װ���и�Ϊ����CuSO4��Һ��һ��ʱ�����ijһ�缫�������� 1.28 g������һ�缫����______________mL������������塣
���𰸡���1������2H++2e-��H2��
��2��ԭ���������Cu2++2e��=Cu
��3��224
��������
�����������1��װ��1�����Ǹ�����ʯī����������������ԭ�����������NO3-�����װ�ã�����CuCl2��Һ��ΪNH4Cl��Һ������������ɫ��ζ�ĵ������壬��ʯī�ϵ缫��Ӧʽ2H++2e-��H2����2��ͼ2�������������䣬�������Ż�����ͭ������ʯī������n�ͣ����װ���������缫��ͬ������ԭ��أ�����װ���ǵ��أ�ʯī��2��������������ʯī��2��Ϊ��������װ����������������ʯī��1�����������缫�Ϸ����ķ�ӦʽΪCu2++2e��=Cu����3��ijһ�缫���� 1.28 gͭ��ת�Ƶ���![]() ������һ�缫��������������ת�Ƶ�����ͬ����������0.01mol������µ����Ϊ224mL��
������һ�缫��������������ת�Ƶ�����ͬ����������0.01mol������µ����Ϊ224mL��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��5���л���ѧ����]
��֪A�Ƿ�������������ֻ��һ��ȡ������A��ȫ��������������������E�ķ���ʽΪC9H8O2����ʹ������Ȼ�̼��Һ��ɫ������������ϳ�����ҩ��H���ϳ�·����ͼ��ʾ��

��֪��

��ش��������⣺
��1��д���л���A�Ľṹ��ʽ��____________���л���D�д��ڵĹ���������Ϊ_______________��
��2��������Ӧ����������ȡ����Ӧ����________________������ţ���
��3���л���H��һ�������¿��Ծۺ��γɸ߷��ӣ�д���þۺ���Ľṹ��ʽ��_______________________��
��4��д��H���������ƴ������µ�ˮ�ⷽ��ʽ��_________________________��
��5���л���E�ж���ͬ���칹�壬д����������������ͬ���칹��Ľṹ��ʽ��_________________��
a�����ڱ����ұ����Ϻ˴Ź�������ֻ��2���ֵ
b��������Cu(OH)2����Һ���ò���ש��ɫ����
c������FeCl3��Һ��ɫ
��6������H�������ϳ�·�ߣ����һ����ʯ�Ͳ�Ʒ��NH2��CH(CH3)2Ϊ��ʼԭ���Ʊ�ҽҩ�м���CH3CONHCH(CH3)2�ĺϳ�·�ߣ�___________________________________________________________________����ע����Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��W��Z �����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯����ͼ��ʾ����֪ W ��һ�ֺ��ص�������Ϊ 18��������Ϊ 10��X��Neԭ�ӵĺ������������� 1��Y �ĵ�����һ�ֳ����İ뵼����ϣ� Z �ķǽ�������ͬ��������Ԫ������ǿ�� ����˵����ȷ���ǣ� ��

A. ����ϼۣ� X��Y��Z��W
B. ����̬�⻯����ȶ��ԣ� Z��Y��W
C. Y ���������� X�� Z ������������Ӧ��ˮ������ܷ�Ӧ
D. �� X�� Z�� W ����Ԫ���γɵĻ�����һ���Ⱥ������Ӽ��ֺ����ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��C5H11OH������ȥ��Ӧʱ�����Եõ�����ϩ�����ֿɷ�������������ô��Ľṹʽ����Ϊ��������
A.
B.![]()
C.
D.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���õ�ΰ�̽�����������ʡ�ʵ��ʱ��NaOH�����ϵμ���Ũ��ˮ��,��������������ס������ΰ塣���ж�ʵ������Ľ�����ȷ����(����)
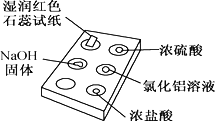
ѡ�� | ʵ������ | ���� |
A | ��ɫʯ����ֽ���� | NH3��������ˮ |
B | Ũ���ḽ���ް��� | NH3��Ũ���������Ӧ |
C | �Ȼ�����Һ����� | NH3��AlCl3��Һ��Ӧ:Al3++3OH-=Al(OH)3�� |
D | Ũ���ḽ���а��� | NH3��ӷ�����HCl��Ӧ:NH3+HCl=NH4Cl |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ�У��ɴ�������������ǣ� ��
A.K+ Na+ OH�� SO42��
B.Mg2+ SO42�� NH4+ Cl��
C.K+ Na+ HCO3�� Cl��
D.K+ Na+ NO3�� CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ס������������������ص�Ԫ�ء��ش��������⣺
(1)N�Ļ�̬ԭ��������Ӳ���е�ԭ�ӹ����Ϊ______��SO2���ӵ�VSEPRģ��������_________��
(2)N��O��P����Ԫ�ص�һ�������ɴ�С��˳����________����̬�⻯�ﰱ(NH3)���(PH3)�ļ��ǽϴ����_________��
(3)SCN����Cԭ�ӵ��ӻ�����Ϊ______��1 mol SCN���к��м�����ĿΪ______NA��
(4)FeO���۵�____Fe2O3���۵�(���������������=��)����ԭ����________________��
(5)��������������Ҫ�أ�
��ԭ�������������ʾ�����ڲ���ԭ�ӵ����λ�á�������һ�ֳ�Ӳ��ĥ��Ϳ����ϣ��侧���ṹ��ͼ��ʾ������ԭ���������AΪ��0��0��0����BΪ��![]() ��
�� ![]() ��0����DΪ��1��1��1������Cԭ�ӵ��������Ϊ______��
��0����DΪ��1��1��1������Cԭ�ӵ��������Ϊ______��

�ھ������������������Ĵ�С����״��Pԭ����Bԭ�ӵ��������Ϊa cm���������ı߳�Ϊ_____cm(�ú�a�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.NaOH��Һ�ܵ��磬����NaOH��Һ�ǵ����
B.����KC1�����磬��KC1�ǵ����
C.��ˮ�ܵ��磬����Cl2�ǵ����
D.CO2��ˮ��Һ�ܵ��磬����CO2�ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�ַdz���Ҫ�Ļ���ԭ�ϣ����ñ����Ժϳɶ����л����������˺ϳɷ��ڡ�PF��֬�������������·�ߣ�����ͼ��
 �ش��������⣺
�ش��������⣺
��1����Ӧ����1��____________��
��2��B�����еĹ����ŵ�����Ϊ_________��B��C�ķ�Ӧ����Ϊ____________��
��3��D�Ľṹ��ʽΪ________������PF��֬�Ļ�ѧ����ʽΪ_______________��
��4���Լ�E��_________��
��5����J�ϳ�����������Ļ�ѧ����ʽΪ _____________________��
��6��д��ͬʱ�������������������������һ��ͬ���칹��__________��
�ٱ����Ͻ���2��ȡ�����Ҵ��ڶ�λ
���ܷ���ˮ�ⷴӦ��������Ӧ������һ��ˮ�������FeCl3��Һ��ɫ
�۴���˳���칹
��7����DΪԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ��Ҷ�ȩ��д���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ�ϻ���ע���Լ��ͷ�Ӧ��������_____________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com