
| A. | CH3CH3→CH3CH2Cl 取代反应 | B. | CH2═CH2→CH3CH2OH 取代反应 | ||
| C. | CH2═CH2→CH2BrCH2Br 加成反应 | D. |  取代反应 取代反应 |
分析 有机物分子中的某些原子或原子团被其他原子或原子团所代替的反应称为取代反应;
有机物分子中的双键或叁键发生断裂,加进(结合)其它原子或原子团的反应称为加成反应,以此解答该题.
解答 解:A.烷烃转换成卤代烃,是和氯气在光照条件下发生的取代反应,故A正确;
B.CH2=CH2中的双键发生断裂,C=C生成C-C,属于加成反应,故B错误;
C.CH2=CH2中的双键发生断裂,双键碳原子上加进了溴原子,属于加成反应,故C正确;
D.苯环中的H被Br原子替代,为取代反应,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质以及转化特点,把握反应类型的判断,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | △H1+△H2=△H3 | B. | △H1-△H2=△H3 | C. | △H1+2△H2=△H3 | D. | △H1-2△H2=△H3 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由H2、I2(g)、HI组成的平衡体系,缩小体积后颜色加深 | |
| B. | 实验室用排饱和食盐水的方法收集氯气 | |
| C. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 | |
| D. | 加压有利于N2和H2在一定的条件下转化为NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 和
和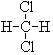 ; ⑦CH3 (CH2) 3CH3和
; ⑦CH3 (CH2) 3CH3和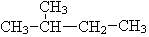
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com