
用食用白醋(醋酸浓度约1mol/L)常温下进行下列实验,能证明醋酸为弱电解质的是( )
|
| A. | 白醋中滴入石蕊试液呈红色 |
|
| B. | 实验测得该白醋的pH为2.3 |
|
| C. | 蛋壳浸泡在白醋中有气体放出 |
|
| D. | 白醋加入豆浆中有沉淀产生 |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
只要说明醋酸在水溶液中部分电离就能证明醋酸是弱电解质,据此分析解答.
解答:
解:A.白醋中滴入石蕊试液变红色,说明白醋属于酸,不能证明其部分电离,所以不能证明醋酸是弱酸,故A错误;
B.实验测得该白醋的pH为2.3,溶液中氢离子浓度小于1mol/L,说明醋酸部分电离,所以能证明醋酸是弱电解质,故B正确;
C.蛋壳浸泡在白醋中有气体放出,说明醋酸酸性大于碳酸,但不能证明醋酸部分电离,所以不能证明醋酸是弱电解质,故C错误;
D.白醋加入豆浆中有沉淀产生,说明白醋是电解质,但不能说明白醋是弱电解质,故D错误;
故选B.
点评:
本题考查了电解质强弱判断,明确弱电解质“部分电离”的特征即可解答,电解质强弱与其溶解性无关,为易错点.


科目:高中化学 来源: 题型:
下列描述中正确的是 ( )。
A.CS2为V形的极性分子
B.ClO3-的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4和SO32-的中心原子均为sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. NaCl固体中含有共价健
B. CO2分子中含有离子健
C. 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16个纵行
D. X2+的核外有18个电子,则X在第四周期第ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
已知aA+、bB2+、cC﹣、dD2﹣四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是()
A. 原子半径:A>B>C>D
B. 原子序数:b>a>c>d
C. 离子半径:D>C>B>A
D. 失电子能力:B>A,得电子能力:D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
|
| A. | 需加热才能发生的反应一定是△H>0 |
|
| B. | CaCO3(s)受热分解为CaO(s)和CO2(g)反应的△S<0 |
|
| C. | 1 mol H2SO4与1 mol Ba(OH)2反应放出的热就是中和热 |
|
| D. | 热化学方程式中的化学计量数表示物质的量,所以可以是分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的氧化产物甲和还原产物乙都能与金属钠反应放出H2,甲和乙反应生成有机物丙,甲和丙都能发生银镜反应,该有机物是( )
|
| A. | CH3CHO | B. | CH3COOH | C. | CH3OH | D. | HCHO |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述或化学用语书写错误的是()
A. 向Fe(0H)3胶体中滴加稀硫酸,先生成红褐色沉淀,后沉淀逐渐溶解
B. 向铜粉中加入稀硫酸,铜粉不溶解,再加入硝酸钾固体,铜粉逐渐溶解
C. 氯碱工业和金属钠的冶炼都用到了NaCl,阳极上发生的电极反应都是:2Cl﹣2e﹣═Cl2↑
D. 向明矾(KAl(SO4)2•12H2O)溶液中滴入Ba(OH)2溶液,SO42﹣恰好完全沉淀时的离子方程式为:Ba2++3OH﹣+Al3++SO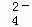 ═BaSO4↓+Al(OH)3↓
═BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中只能表示一个化学反应的是 ( )。
①Ag++Cl-===AgCl↓ ②Ba2++2OH-+2H++SO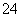 ===BaSO4↓+2H2O ③CaCO3+2H+===CO2↑+H2O+Ca2+ ④Fe+Cu2+===Fe2++Cu ⑤Cl2+H2O===H++Cl-+HClO
===BaSO4↓+2H2O ③CaCO3+2H+===CO2↑+H2O+Ca2+ ④Fe+Cu2+===Fe2++Cu ⑤Cl2+H2O===H++Cl-+HClO
A.①③ B.⑤
C.②⑤ D.④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com