
| A. | 6s | B. | 2d | C. | 3p | D. | 7f |
分析 根据每一能层含有的能级数与其能层数相等,且每一能层都是从S能级开始,第一层(K层)上只有1S亚层,第二电子层(L层)只有2s和2p亚层,第三电子层(M层)只有3s、3p和3d亚层,第四电子层(N层)只有4s、4p、4d和4f亚层,据此分析解答.
解答 解:A.s亚层在每一层上都有,故A正确;
B.第二能层含有2s、2p两个能级,所以不存在2d能级,故B错误;
C.第三能层含有3s、3p、3d三个能级,所以存在3p能级,故C正确;
D、f能级至少在第四层及以上,故存在7f能级,故D正确;
故选B.
点评 本题考查了能层中的能级,从能层数与能级数之间的关系分析解答,属于基础题,难度不大.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:实验题
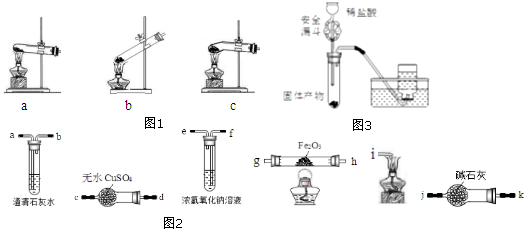
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
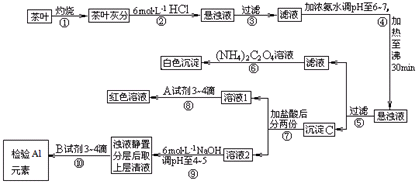
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液很快褪色 | B. | 溶液不褪色 | C. | 出现沉淀 | D. | 不出现沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
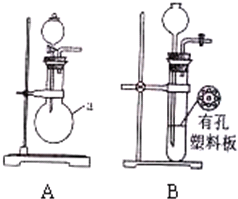 (1)用A装置制SO2,化学反应方程式为Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑.
(1)用A装置制SO2,化学反应方程式为Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
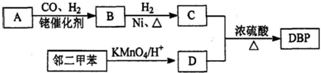

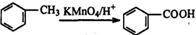


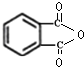 .
.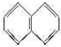 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
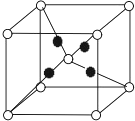 A、B、C、D、E、F、G 原子序数依次增大,A 与 B 不同周期,基态 B 原子核外电子占据 3 个能级,每个能级上电子数相等.D 能形成两种阴离子且电子总数分别为 10、18.E 是短周期电负性最强的元素.基态 F 的价层电子排布式为 ns xnp y,有 n=x+y.基态的+1 价 G 离子核外电子恰好排满三个电子层.
A、B、C、D、E、F、G 原子序数依次增大,A 与 B 不同周期,基态 B 原子核外电子占据 3 个能级,每个能级上电子数相等.D 能形成两种阴离子且电子总数分别为 10、18.E 是短周期电负性最强的元素.基态 F 的价层电子排布式为 ns xnp y,有 n=x+y.基态的+1 价 G 离子核外电子恰好排满三个电子层.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH3易液化,液氨常用作制冷剂 | |
| B. | 与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 | |
| C. | 铵盐受热易分解,因此贮存氮肥时要密封保存,并放在阴凉通风处 | |
| D. | 不能用稀HNO3和金属反应制取氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com