
| A、升温 |
| B、加水 |
| C、加入NaOH溶液 |
| D、加入0.1mol/L HCl |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B、AgCl难溶于水,溶液中没有Ag+和Cl- |
| C、在AgCl的澄清饱和溶液中,只要向其中加入NaCl溶液,一定会有沉淀生成 |
| D、向含有AgCl沉淀的悬浊液中加入NaCl固体,AgCl的溶解度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Al3+、Cl-、AlO2- |
| B、Mg2+ NO3- Fe2+、H+ |
| C、Fe3+、SO42-、Na+、SCN- |
| D、K+、Na+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| B、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、R原子的电子层数比N的电子层数多1 |
| B、R元素的最高正化合价与NO3-中的N的化合价相等 |
| C、RO3-和NO3-都只能被还原,不能被氧化 |
| D、R和N为同族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
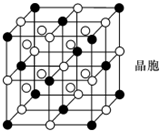 A,B,C,D,E,F都是短周期元素,原子序数依次增大,B,C同周期且相邻,A,D同主
A,B,C,D,E,F都是短周期元素,原子序数依次增大,B,C同周期且相邻,A,D同主x- 6 |
 表示)位于该正方体的顶点和面心.该化合物的化学式是
表示)位于该正方体的顶点和面心.该化合物的化学式是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L的硫酸 |
| B、0.1mol/L的碳酸 |
| C、0.1mol/L的醋酸 |
| D、0.1mol/L的盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com