
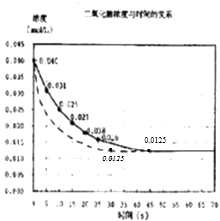
【题目】二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡(NO2浓度约为0.0125molL﹣1).如图中的曲线表示二氧化氮分解反应在前25s内的反应进程. 
(1)写出反应的化学方程式 .
(2)在10s内氧气的反应速率 .
(3)若反应延续至70s,请在图中用实线画出25s至70s的反应进程曲线;
(4)若在反应开始时加入催化剂(其他条件都不变),请在图上用虚线画出加催化剂的反应进程曲线.
【答案】
(1)2NO2?2NO+O2
(2)7.5×10﹣4mol/(L?s)
(3)
(4)
【解析】解:(1)二氧化氮在加热条件下能够分解成一氧化氮和氧气,达到平衡时NO2浓度约为0.0125molL﹣1 , 说明为可逆反应,反应方程式为:2NO22NO+O2 , 所以答案是:2NO22NO+O2;(2)由图可知,10秒内NO2的浓度变化为0.04mol/L﹣0.015mol/L=0.025mol/L,故v(NO2)= ![]() =0.0015mol/(Ls),对于2NO22NO+O2 , 速率之比等于化学计量数之比,所以v(O2)=
=0.0015mol/(Ls),对于2NO22NO+O2 , 速率之比等于化学计量数之比,所以v(O2)= ![]() v(NO2)=
v(NO2)= ![]() ×0.0015mol/(Ls)=7.5×10﹣4mol/(Ls),所以答案是:7.5×10﹣4mol/(Ls);(3)25s后二氧化氮浓度继续减小,该反应进行到45秒时,达到平衡是NO2浓度约为0.0125mol/L,实线画出25秒至70秒的反应进程曲线为
×0.0015mol/(Ls)=7.5×10﹣4mol/(Ls),所以答案是:7.5×10﹣4mol/(Ls);(3)25s后二氧化氮浓度继续减小,该反应进行到45秒时,达到平衡是NO2浓度约为0.0125mol/L,实线画出25秒至70秒的反应进程曲线为  ,所以答案是:
,所以答案是:  ; 3)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,用虚线画出加催化剂后的反应进程曲线为
; 3)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,用虚线画出加催化剂后的反应进程曲线为 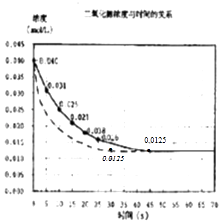 ,所以答案是:
,所以答案是:  .
.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效),以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】有关铜与浓硫酸的反应下列说法错误的是
A. 该反应中氧化剂与还原剂物质的量之比为1:1
B. 浓硫酸在反应中既体现出氧化性,又体现出酸性
C. 标准状况下,lmol铜和2mol浓硫酸充分反应可得22.4L气体
D. 1mol铜和足量浓硫酸反应,转移电子个数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的锌与100mL 18.5mol/L H2SO4充分反应后,锌完全溶解,同时生成气体A 22.4L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中错误的是( )
A.气体A为SO2和H2的混合物
B.反应中共消耗Zn 65g
C.气体A中SO2和H2的体积比为1:4
D.反应中共转移电子2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,E,F为原子序数依次增大的短周期主族元素.A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级且每个能级上的电子数相同;A与C形成的分子为三角锥形;D原子p轨道上成对的电子总数等于未成对的电子总数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F.
(1)A,C形成的分子极易溶于水,与该分子互为等电子体的阳离子为 .
(2)比较E、F的第一电离能:E(填“>”或“<”)F.
(3)BD2在高温高压下所形成的晶胞如图所示.该晶体的类型属于(填“分子”“原子”“离子”或“金属”)晶体,该晶体中B原子的杂化形式为 . 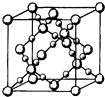
(4)单质F与强碱溶液反应有[F(OH)4]﹣生成,则[F(OH)4]﹣中存在(填字母). a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(5)Cu晶体是面心立方体,立方体的每个面5个Cu原子紧密堆砌,已知每个Cu原子的质量为a g,Cu原子半径为d cm,求该晶体的密度为gcm﹣3 . (用含a、d的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3和HNO3是重要的工业产品,下图为合成氨以及氨氧化制硝酸的流程。

(1)合成塔中发生反应的化学方程式是_______________________________
从氨分离器中又回到合成塔中的物质是_________________。
(2)氧化炉中发生反应的化学方程式是_________________________________________
(3)尾气中的少量NO、NO2可以用NH3来处理,在催化剂作用下生成无污染的气体,写出NO2和 NH3反应的化学方程式__________________________________________________
当有5.6L NO2被还原时,转移电子的物质的量为 ________________mol.
(4)氧化炉中出来的气体,先降温再进入吸收塔,吸收塔中通入空气的作用是_________________.若进入吸收塔的气体的体积分数为NO210.0%,NO 1.32%,其余为N2、水蒸气等.当进入吸收塔中气体为10m3时,最少需要空气的体积为_____________m3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,1mol化学键分解成气态原子所需要的能量用E表示,结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ·mol1) | 436 | 157 | 568 | 432 | 298 |
A. 表中最稳定的共价键是H-F
B. 1mol H2(g)与1mol F2(g)生成2molHF(g)放出25kJ的能量
C. 432kJ·mol1>E(H-Br)>298kJ·mol1
D. 1mol H2(g)分解成2mol H(g) 需吸收436kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当增大压强时,下列化学反应速率不会变大的是( )
A.碘蒸气和氢气化合生成碘化氢
B.稀硫酸和氢氧化钡溶液反应
C.二氧化碳通入澄清石灰水
D.氨的催化氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com