
| A. | 都具有强氧化性 | |
| B. | 分别露置在空气中,容器内溶质的物质的量浓度都降低 | |
| C. | 常温下都可以储存于铝制槽罐中 | |
| D. | 和碳反应中都表现出强氧化性和强酸性 |
分析 A、浓硝酸和浓硫酸都具有强氧化性;
B、浓硫酸具有吸水性,浓硝酸具有挥发性;
C、常温下,都能与铝发生钝化现象;
D、和碳反应中只表现出强氧化性;
解答 解:A、浓硝酸和浓硫酸都具有强氧化性,故A正确;
B、浓硫酸具有吸水性,浓硝酸具有挥发性,所以敞口露置于空气中,一段时间后,容器内的溶质的物质的量浓度都降低,但浓硫酸质量增加、浓硝酸质量减少,故B正确;C、常温下,浓硝酸和浓硫酸都能与铝发生钝化现象而阻止进一步反应,所以常温下都可以储存于铝制槽罐中,故C正确;
D、和碳反应中只表现出强氧化性,而无酸性,故D错误;
故选D.
点评 本题考查了浓硝酸和浓硫酸的性质,知道二者都具有强氧化性,常温下能与铁或铝发生钝化现象,知道二者性质的差异性,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol•L-1 | B. | 0.4 mol•L-1 | C. | 0.3 mol•L-1 | D. | 0.2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁条燃烧可用泡沫灭火器灭火 | |
| B. | 工业上电解氯化钠、氯化镁溶液制取可以得到金属钠、镁 | |
| C. | 通常情况下,铁是银白色金属,硬度较大,可以被磁石吸引 | |
| D. | 铜能与氯化铁溶液反应,该反应可以用于印刷电路板的制作 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5Br和NaOH溶液混合共热 | |
| B. | 乙醇和NaOH溶液混合共热 | |
| C. | 一溴丁烷与的NaOH的丁醇溶液混合共热 | |
| D. | 氯苯与NaOH溶液混合共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中的能量变化都表现为热量变化 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 反应物和生成物所具有的总能量决定了反应是放热还是吸热 | |
| D. | 向醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深,说明盐类水解是放热的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2不溶于水,但能溶于浓NH4Cl溶液中 | |
| B. | 水垢中含有的CaSO4,先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,再用酸除去 | |
| C. | 洗涤BaSO4沉淀时,用稀硫酸洗涤BaSO4沉淀比用蒸馏水洗涤损失少 | |
| D. | FeCl3溶液中混有FeCl2,常加入少量的H2O2,使Fe2+氧化为Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色,①不能(填“能”或“不能”)确定产物中铁元素的价态 |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液 | ②若KMnO4溶液的紫红色褪去或变浅,则说明产物中含+2价铁元素,若KMnO4溶液不褪色或不变浅,则说明产物中不含+2价铁元素 |
| 步骤3:③另取少量溶液,滴加KSCN溶 | ③若溶液变为红色,说明产物中含+3价铁元素;若溶液颜色无明显变化,则说明产物中不含+3价的铁元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
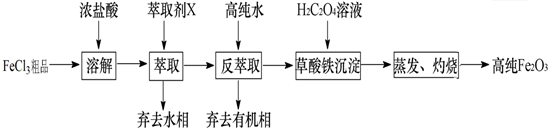
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com