
科目:高中化学 来源: 题型:
向三份25mL等浓度的盐酸中分别加入质量不等的NaHCO3和KHCO3的混合物,测得产生气体的体积(不考虑气体溶解)如表中所示:下列说法正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 3 |
| 2 |
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| 3 |
| 2 |

查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058

(1)将气体b中的Cu粉小心倒入烧瓶中,要使Cu粉发生反应,是否一定需要对反应混合物进行加热(填“是”或“否”) ,发生反应的化学方程式是 ;充分反应后Cu粉有剩余,在反应过程中可观察到的现象是:① ,② ,③ ,④ ;
(2)欲加快铜与硝酸的反应速率,可采用多种不同的措施,若采用化学试剂法,下列试剂中可以使用的是(填代号) ;
A.蒸馏水 B.无水醋酸钠 C.石墨 D.AgNO3(少量)
(3)将烧瓶不断振荡,发现气球逐渐变小,直至被吸入烧瓶内,发生这一现象的原因是(用化学方程式表示) 。
(4)打开弹簧夹将CO2推入干燥管内继续振荡,使气体与气体、气体与液体间充分接触,可使剩余铜粉完全溶解,上述整个过程用一个总化学方程式表示则为:
,在此过程中,至少需要CO2 mL。(标准状况)
查看答案和解析>>
科目:高中化学 来源:山东省威海市2010-2011学年高一下学期期末模块考试化学试卷 题型:022
课本“交流·研讨”栏目有这样一组数据:破坏1 mol氢气中的化学键需要吸收436 kJ能量;破坏1/2 mol氧气中的化学键需要吸收249 kJ的能量;形成水分子中1 mol H-O键能够释放463 kJ能量.
下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在下边的横线上.

①________kJ
②________kJ
③________kJ
查看答案和解析>>
科目:高中化学 来源:2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷 题型:计算题
将4 mol SO 与2 mol O
与2 mol O 放入4L的密闭容器中
放入4L的密闭容器中 ,在一定条件下发生反应:
,在一定条件下发生反应:
2SO (g)+O
(g)+O (g)
(g)  2SO
2SO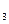 (g),达到平衡时混合物总的物质的量为5 mol 。求:
(g),达到平衡时混合物总的物质的量为5 mol 。求:
(1) 该温度下的平衡常数K。(2)平衡时SO 的转化率。
的转化率。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com