
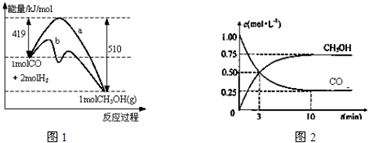
���� ��1������ͼ�з�Ӧ�Ļ�ܵĴ�С�������Ƿ�ʹ�ô��������÷�Ӧǰ�����������������Ӧ�������仯��
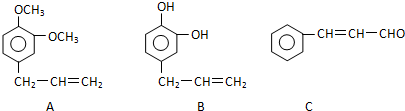
��2��A����ͼ2����ת����CO��ƽ��ʱCO������������
B������COŨ�ȣ���ٽ�������ת������������ת���ʽ��ͣ�
C���÷�ӦΪ��Ӧǰ��ѹǿ���ȵķ�Ӧ��
D���ٳ���1molCO��2molH2��������䣬��ѹǿ����ƽ�������ƶ���
��3����ͼ2������CO��ʾ�ķ�Ӧ���ʣ������÷�Ӧ����֮�ȵ��ڻ�ѧ������֮�������������ķ�Ӧ���ʣ����ø�����ƽ���Ũ�������㻯ѧƽ�ⳣ���������¶����ߣ�ƽ�������ƶ�����Ӧ���Ũ�������������Ũ�ȼ��٣�ƽ�ⳣ����С��
��4�����ݸ�˹������д�Ȼ�ѧ����ʽ��
��5���״�ȼ�ϵ���У��״��Ӹ���ͨ�룬�ڷ�Ӧ��ʧ���ӱ���������������������̼������Ӻ�ˮ��
��� �⣺��1����ͼ��֪������b�����˷�Ӧ����Ļ�ܣ���bʹ���˴������ָ÷�Ӧ�з�Ӧ������������������������������÷�ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ��b�����ȣ�
��2��A����ͼ2��֪����0.75mol/LCH3OH����Ӧ��0.75mol/LCO��ƽ��ʱ��0.25mol/LCO����CO����ʼ���ʵ���Ϊ��0.75mol/l+0.25mol/L����2L=2mol����A��ȷ��
B������COŨ�ȣ���ٽ�������ת����������ת��������CO��ת���ʼ�С����B����
C���÷�ӦΪ��Ӧǰ��ѹǿ���ȵķ�Ӧ����ѹǿ����ʱ���÷�Ӧ�ﵽƽ��״̬����C��ȷ��
D���ٳ���1molCO��2molH2��������䣬��ѹǿ����ƽ�������ƶ����ٴδﵽƽ��ʱn��CH3OH��/n��CO��������D����
��ѡ��AC��
��3����ͼ2��֪����Ӧ�м�С��CO��Ũ��Ϊ1mol/L-0.25mol/L=0.75mol/L��10minʱ�ﵽƽ�⣬
����CO��ʾ�Ļ�ѧ��Ӧ����Ϊ$\frac{0.75mol/L}{10min}$=0.075mol•L-1•min-1��
��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v��H2��=0.075mol•L-1•min-1��2=0.15mol•L-1•min-1��
CO��g��+2H2��g��?CH3OH��g��
��ʼ��mol/L�� 1 2 0
ת����mol/L�� 0.75 1.5 0.75
ƽ�⣨mol/L�� 0.25 0.5 0.75
��ѧƽ�ⳣ��K=$\frac{0.75}{0.25����0.5��^{2}}$=12��
���¶����ߣ�ƽ�������ƶ�����Ӧ���Ũ�������������Ũ�ȼ��٣�ƽ�ⳣ����С��
�ʴ�Ϊ��0.15mol•L-1•min-1��12�� ��С��
��2����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H1=-1275.6kJ/mol
��2CO ��g��+O2��g��=2CO2��g����H2=-566.0kJ/mol
��H2O��g��=H2O��l����H3=-44.0kJ/mol
�ɸ�˹���ɢ�-��+�ۡ�4���ã�2CH3OH��l��+2O2��g��=2CO ��g��+4H2O��l����H=-885.6KJ/mol��
�ʴ�Ϊ��CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442.8 kJ/mol��
��5���ڼ״�ȼ�ϵ���У���������ȼ�ϼ״�����ʧ���ӵ�������Ӧ���ڼ��Ի����£��缫��ӦΪ��CH3OH+8OH--6e-�TCO32-+6H2O��
�ʴ�Ϊ��CH3OH+8OH--6e-�TCO32-+6H2O��
���� ���⿼�黯ѧ��Ӧ���ʡ���ѧƽ�⼰�����仯��ѧ��Ӧע��ͼ�������������������⣬ͼ���е���Ϣ�ǽ����Ĺؼ���


 �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
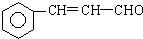 +5H2$\stackrel{һ��������}{��}$
+5H2$\stackrel{һ��������}{��}$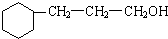 ��
��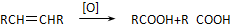 д��C��ǿ���������������ɵ��л�������Ľṹ��ʽ
д��C��ǿ���������������ɵ��л�������Ľṹ��ʽ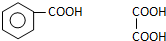 ��
��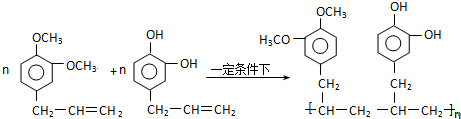 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��й¶�ı�����ʯ��ˮ�кͱ��þƾ���ϴ���ķ����� | |
| B�� | ��Ũ��Һ��Ƥ����ǿ�ҵĸ�ʴ�ԣ��������մ��Ƥ���ϣ�Ӧ�����þƾ���ϴ | |
| C�� | ����ˮ�е��ܽ�����¶ȵ����{��������65�������ˮ������Ȼ��� | |
| D�� | ̼��������Һ�е��˱��ӵ�ˮ��Һ���ų�������̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
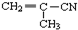 ��
��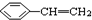 ��
��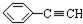 ��CH3-CH=CH-CN ��CH2=CH-CH=CH2�����п����ںϳɸ߷��Ӳ��ϣ��ṹ��ͼ��ʾ������ȷ���Ϊ��������
��CH3-CH=CH-CN ��CH2=CH-CH=CH2�����п����ںϳɸ߷��Ӳ��ϣ��ṹ��ͼ��ʾ������ȷ���Ϊ��������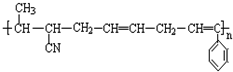
| A�� | �٢ڢ� | B�� | �٢ڢ� | C�� | �ڢܢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ö��Ե缫��ⱥ��ʳ��ˮʱ�������ĵ缫��ӦʽΪ��2Cl-�TCl2��+2e- | |
| B�� | ����ȼ�ϵ�صĸ�����Ӧʽ��O2+2H2O+4e-�T4OH- | |
| C�� | ��ͭ����ʱ�����Դ�����������Ǵ�ͭ���缫��ӦʽΪ��Cu�TCu2++2e- | |
| D�� | ���������绯ѧ��ʴ��������Ӧʽ��Fe�TFe2++2e- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȩ������ | B�� | �������������� | ||
| C�� | CH3CH2CHO��CH3COCH3 | D�� | CH3CH2CH2OH��CH3OCH2CH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ö��Ե缫���һ��Ũ�ȵ�����ͭ��Һ��һ��ʱ�����0.1molCu��OH��2��ǡ�ûָ������ǰ��Ũ�Ⱥ�pH�����������ת�Ƶ�����Ϊ0.4mol | |
| B�� | ����ĵ��뷽��ʽΪ��H3PO4=H++H2PO4- | |
| C�� | ���ʱ���ֵ����㶨�����¿�֪�ӿ췴Ӧ���� | |
| D�� | ��ӦNH3��g��+HCl��g���TNH4Cl��s���������¿��Է����У���÷�Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����봿����Һ��Ϸ�Ӧ�����ӷ���ʽ��2C6H5OH+CO32-��CO2��+H2O+2C6H5O- | |
| B�� | �����鷢��ˮ�ⷴӦ�����ӷ���ʽ��CH3CH2Br+OH-$��_{��}^{H_{2}O}$CH3CH2O-+H++Br- | |
| C�� | ��ϩ��ˮ�����ӳɷ�Ӧ�Ļ�ѧ����ʽ��CH2=CH-CH3+H2O$��_{��}^{����}$CH3-O-CH2-CH3 | |
| D�� | ����ϡ��Һ�м��뱥����ˮ��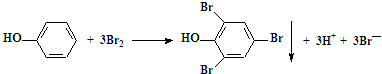 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com