
| A.N、O、F | B.N、P、As | C.K、Na、Li | D.Cl、O、H |
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源:不详 题型:单选题
| A.氢化物沸点:HI>HBr>HCl>HF | B.离子半径:K+>Cl->S2- |
| C.分子稳定性:HF>HCl>HBr>HI | D.单质熔点:Li<Na<K<Rb |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.砹(At)为有色固体,HAt不稳定 |
| B.铊(T1)是铝的同族元素,原子核外有6个电子层,推测T1(OH)3是两性氢氧化物 |
| C.已知锶Sr与镁同族且原子半径大于钙,硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)比硫化氢稳定性差 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.零族元素的单质在常温下都是气体 |
| B.第ⅡA族元素都是金属元素 |
| C.Fe位于周期表的第四周期,第ⅧB族 |
| D.第ⅦA族元素的单质在常温下有气态、液态、固态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有① | B.只有② | C.只有③ | D.①②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 D、A与G均可形成18e—的化合物。两种化合物在水溶液中反应的化学方程式为:
D、A与G均可形成18e—的化合物。两种化合物在水溶液中反应的化学方程式为: 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
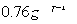 ;W的质子数是X、Y、Z、M四种元素质子数之和的
;W的质子数是X、Y、Z、M四种元素质子数之和的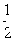 。下列说法正确的是
。下列说法正确的是| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳、氮原子构成网状结构的原子晶体 |
| B.膜中C—N键的键长比金刚石中的C—C键的键长短 |
| C.碳、氮同属非金属元素,化合时放出大量热 |
| D.由相邻主族的非金属元素所形成的化合物都比单质的硬度大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com