
·ÖĪö ĻąĶ¬Ģõ¼žĻĀĘųĢåµÄĢå»ż·ÖŹżµČÓŚĘäĪļÖŹµÄĮæ·ÖŹż£¬¾Ż“Ė½įŗĻm=nM¼ĘĖć³ö»ģŗĻĘųĢåµÄ×ÜÖŹĮ棻ĄūÓĆ¹«Ź½¦Ń=$\frac{{m}_{×Ü}}{V}$¼ĘĖć³ö»ģŗĻĘųĢåŌŚ±ź×¼×“æöĻĀµÄĆÜ¶Č£®
½ā“š ½ā£ŗĻąĶ¬Ģõ¼žĻĀĘųĢåµÄĢå»ż·ÖŹżµČÓŚĘäĪļÖŹµÄĮæ·ÖŹż£¬0.500ĦøĆ»ģŗĶĘųĢåµÄÖŹĮæĪŖ£ŗ0.500mol”Į£Ø16g/mol”Į80%+28g/mol”Į15%+30g/mol”Į05%£©=9.25g£»
±ź×¼×“æöĻĀ0.500mol»ģŗĻĘųĢåµÄĢå»żĪŖ£ŗ22.4L/mol”Į0.500mol=11.2L£¬Ōņ»ģŗĻĘųĢåµÄĆܶČĪŖ£ŗ¦Ń=$\frac{{m}_{×Ü}}{V}$=$\frac{9.25g}{11.2L}$=0.826g/J£¬
“š£ŗ0.500moløĆ»ģŗĻĘųĢåµÄÖŹĮæĪŖ9.25g£¬±ź×¼×“æöĻĀµÄĆܶČĪŖ0.826g/L£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ģŗĻĪļµÄ¼ĘĖć£¬ĢāÄæÄŃ¶Č²»“ó£¬Ć÷Č·ĪļÖŹµÄĮæÓėĘųĢåĦ¶ūĢå»ż”¢Ä¦¶ūÖŹĮæÖ®¼äµÄ¹ŲĻµĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÓŠĄūÓŚĢįøßѧɜµÄ»Æѧ¼ĘĖćÄÜĮ¦£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪļÖŹ | MnS | CuS | PbS |
| Ksp | 2.5”Į10-13 | 6.3”Į10-36 | 8.0”Į10-28 |
| ĪļÖŹ | Fe£ØOH£©3 | Fe£ØOH£©2 | Mn£ØOH£©2 |
| æŖŹ¼³ĮµķpH | 2.7 | 7.6 | 8.3 |
| ĶźČ«³ĮµķpH | 3.7 | 9.6 | 9.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 150 mL 1 mol•L-1 NaClČÜŅŗ | B£® | 75 mL 2 mol•L-1 NH4ClČÜŅŗ | ||
| C£® | 150 L 3 mol•L-1 KClČÜŅŗ | D£® | 75 mL 1 mol•L-1 CaCl2ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1LČÜŅŗÖŠŗ¬Ņõ”¢ŃōĄė×Ó×ÜŹżŹĒ0.6NA | |
| B£® | 500mLČÜŅŗÖŠ¦¢a2+µÄÅØ¶ČŹĒ0.2mol•L-1 | |
| C£® | 500mLČÜŅŗÖŠNO-3µÄÅØ¶ČŹĒ0.4mol•L-1 | |
| D£® | 1LČÜŅŗÖŠŗ¬ÓŠ0.2NAøöNO-3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
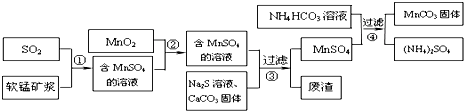
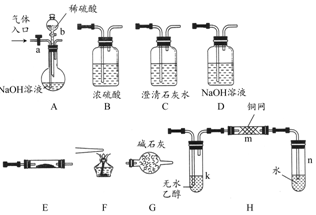 ČēĶ¼ĖłŹ¾ĪŖ³£¼ūĘųĢåÖʱø”¢·ÖĄė”¢øÉŌļŗĶŠŌÖŹŃéÖ¤µÄ²æ·ÖŅĒĘ÷×°ÖĆ£Ø¼ÓČČÉč±ø¼°¼Š³Ö¹Ģ¶Ø×°ÖĆ¾łĀŌČ„£©£¬Ēėøł¾ŻŅŖĒóĶź³ÉĻĀĮŠø÷Ģā£ØŅĒĘ÷×°ÖĆæÉČĪŅāŃ”ÓĆ£¬±ŲŅŖŹ±æÉÖŲø“Ń”Ōń£©£®
ČēĶ¼ĖłŹ¾ĪŖ³£¼ūĘųĢåÖʱø”¢·ÖĄė”¢øÉŌļŗĶŠŌÖŹŃéÖ¤µÄ²æ·ÖŅĒĘ÷×°ÖĆ£Ø¼ÓČČÉč±ø¼°¼Š³Ö¹Ģ¶Ø×°ÖĆ¾łĀŌČ„£©£¬Ēėøł¾ŻŅŖĒóĶź³ÉĻĀĮŠø÷Ģā£ØŅĒĘ÷×°ÖĆæÉČĪŅāŃ”ÓĆ£¬±ŲŅŖŹ±æÉÖŲø“Ń”Ōń£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ÓŠ¢Ł¢Ś | B£® | Ö»ÓŠ¢Ś¢Ü | C£® | Ö»ÓŠ¢Ś¢Ū¢Ü | D£® | Ö»ÓŠ¢Ł¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
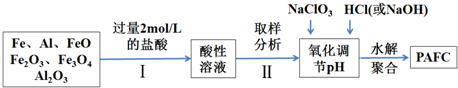
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
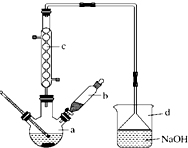 äå±½ŹĒŅ»Öֻƹ¤ŌĮĻ£¬ŹµŃéŹŅŗĻ³Éäå±½µÄ×°ÖĆŹ¾ŅāĶ¼ČēĶ¼ĖłŹ¾£¬ĪļÖŹµÄÓŠ¹ŲŹż¾ŻŠÅĻ¢Čē±ķ£¬Ēė°“ĻĀĮŠŗĻ³É²½Öč»Ų“šĪŹĢā£ŗ
äå±½ŹĒŅ»Öֻƹ¤ŌĮĻ£¬ŹµŃéŹŅŗĻ³Éäå±½µÄ×°ÖĆŹ¾ŅāĶ¼ČēĶ¼ĖłŹ¾£¬ĪļÖŹµÄÓŠ¹ŲŹż¾ŻŠÅĻ¢Čē±ķ£¬Ēė°“ĻĀĮŠŗĻ³É²½Öč»Ų“šĪŹĢā£ŗ| ±½ | äå | äå±½ | |
| ĆܶČ/g?cm-3 | 0.88 | 3.10 | 1.50 |
| ·Šµć/”ę | 80 | 59 | 156 |
| Ė®ÖŠČܽā¶Č | Ī¢ČÜ | Ī¢ČÜ | Ī¢ČÜ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com