
�л��ϳ��г��õ��٣�����̿����������ʹ�ã��ᱻ�����л��������������Ⱦ��ʧȥ���ԣ���Ϊ�ϴ�����һ���ɷϴ�����ȡPdCl2�Ĺ����������£�

��1��������1��ͨ�������Ŀ����ʹ�л����������̿�ȿ�ȼ��ͨ��ȼ�ն�������ͨ��������෴��������ʵ��Ŀ�ģ���ԭ���� ��
��2�������ڷ�Ӧ�б�����Ϊ������̼��д��������PdO��Ӧ�Ļ�ѧ����ʽ��___ ��
��3����Ũ��ˮʱ����ת��Ϊ������[Pd��NH3��4]2+����ʱ���Ĵ�����ʽ�� ��д��ѧʽ����
��4������Ũ��ˮ�Ĺ����У���Ҫ������Һ��pHΪ8��9��ʵ���Ҽ����ҺpH�IJ��������ǣ�
��
��5��������2����Ŀ���ǣ� ��
��6���뱺��2�������������Ԫ����ͬ�Ļ������� ��������������γ�һ�ֻ����ͼ���ȼ�ϵ�أ��为����ӦʽΪ
��7�� Pd�м�����ˮ�ķ�Ӧ���Ա�ʾΪPd+HCl+HNO3��A+B��+H2O��δ��ƽ��������BΪ��ɫ�ж����壬�������ڿ����в����ȶ����ڣ�A�к�������Ԫ�أ�����PdԪ�ص���������Ϊ42��4%��HԪ�ص���������Ϊ0��8%����A�Ļ�ѧʽΪ ��
��֪ʶ�㡿�Ʊ�ʵ�鷽������ơ�������ԭ��Ӧ���ⶨ��ҺpH�ķ��� B3 H2 J4
���𰸽�������1�������Ŀ�������ߴ������ȣ�ʹ��Ӧ�����¶ȹ��ͣ��������ܷ�����Ӧ����2�֣�
��2�� HCOOH��PdO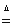 Pd��CO2����H2O��2�֣�
Pd��CO2����H2O��2�֣�
��3��Fe(OH)3��2�֣�
��4���ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ������ɫ����ɫ������pH��2�֣�
��5���Ѱ���ʹ Pd(NH3)2Cl2����PdCl2����2�֣�
��6��N2H4����1�֣�N2H4+4OH����4e��==N2��+4H2O��2�֣�
��7�� H2PdCl4��2�֣�
��������1��Ϊ��ʹ�л���ȿ�ȼ����ȼ�գ�Ҫ�����������������ͨ�������������Ŀ�������ߴ������ȣ�ʹ��Ӧ�����¶ȹ��ͣ��������ܷ�����Ӧ��
��2�����������Ϣ֪�����ᱻ�������ɶ�����̼������������ﱻ��ԭ���ɽ������ʣ�ͬʱ�÷�Ӧ�л�����ˮ����Ӧ����ʽΪ��HCOOH+PdO═Pd+CO2��+H2O��
��3����Ũ��ˮ����pHΪ8��9����Һ�ʼ��ԣ���ǰ���������ǿ�������������Ĵ�����ʽ��Fe(OH)3
��4��ʵ��������pH��ֽ�����Һ��pH�IJ��������ǣ��ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ�Ȼ��pH��ֽ�����ɫ���Աȣ�
��5�����������Ϣ֪����Ӧ����Pd��NH3��2Cl2����������PdCl2��������2����Ŀ���Ƿ����ֽⷴӦ���õ����
��6�����շ���ʽΪ:Pd��NH3��2Cl2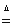 2NH3��+PdCl2
2NH3��+PdCl2
�백�����Ԫ����ͬ�Ļ�������N2H4��������������γ�һ�ֻ����ͼ���ȼ�ϵ�أ��为����ӦʽΪN2H4+4OH����4e��==N2��+4H2O��
��7��Pd�м�����ˮ�ķ�Ӧ���Ա�ʾΪPd+HCl+HNO3-��A+B��+H2O��δ��ƽ��������BΪ��ɫ�ж����壬�������ڿ����в����ȶ����ڣ���B��һ��������A�к�������Ԫ�أ�����PdԪ�ص���������Ϊ42.4%��HԪ�ص���������Ϊ0.8%������Ԫ���غ�֪ʣ�������Ԫ�أ���Ԫ�ص���������Ϊ1-42.4%-0.8%=56.8%��Pdԭ�ӡ���ԭ�Ӻ���ԭ�Ӹ�����Ϊ����42.4%/106.4��:��0.8%/1������56.8%/35.5��=1:2:4����A�Ļ�ѧʽΪ��H2PdCl4
��˼·�㲦�����⿼�����Ʊ���������ƣ��漰��ѧʽ��ȷ����������ԭ��Ӧ��pH�IJⶨ��֪ʶ�㣬����ԭ���غ㼰ԭ�Ӹ�����ȷ����ѧʽ��


 �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д� ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��һ��������2SO2(g)��O2(g)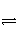
 2SO3(g)����H����Q kJ��mol��1����һ�ܱ������м���2 mol SO2��1 mol O2����ƽ��ʱSO2��ת����Ϊ90%���ų�������ΪQ1������һ��ͬ�����м���2 mol SO3������ͬ�����£���ƽ��ʱ���յ�����ΪQ2�������й�ϵ����ȷ����(����)����������������������������������
2SO3(g)����H����Q kJ��mol��1����һ�ܱ������м���2 mol SO2��1 mol O2����ƽ��ʱSO2��ת����Ϊ90%���ų�������ΪQ1������һ��ͬ�����м���2 mol SO3������ͬ�����£���ƽ��ʱ���յ�����ΪQ2�������й�ϵ����ȷ����(����)����������������������������������
A��Q>Q1>Q2 B��Q1>Q2>Q C��Q1>Q>Q2 D��Q1��Q2>Q
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA���������ӵ�������ֵ������˵������ȷ����
A��1L 1mol·L-1��CH3COOH��Һ�к���NA��������
B����NA��Na+��Na2O�ܽ���1Lˮ�У�Na+�����ʵ���Ũ��Ϊ1mol·L-1
C��0.1mol�������ڹ��������г��ȼ�գ����ɵĻ���������������Ϊ0.15NA
D����VLCO��NO�Ļ�������к��е���ԭ�Ӹ���Ϊ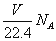
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����
A��Ũ��ˮ�еμ�FeCl3������Һ���Ƶ�Fe(OH)3����
B��CH3COONa��Һ�еμ�����Ũ�����c(CH3COO��)����
C��Ca(HCO3)2��Һ�����NaOH��Һ��Ӧ���Ƶ�Ca(OH)2
D��25��ʱCu(OH)2��ˮ�е��ܽ�ȴ�������Cu(NO3)2��Һ�е��ܽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������Ӧ�ò����ý����֪ʶ���͵���(����)
A��������˥�ߵȼ��������ѪҺ�ж���������ѪҺ����������
B���������������һ������磬������NH4+��Ӫ�����ӣ�ʹ�������б�������
C��ˮ�ࡢұ�����ø�ѹ���ȥ�����̳������ٶԿ�������Ⱦ
D���Ȼ�����Һ�м���̼������Һ����ְ�ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�����µ������£�pH��Ϊ5��H2SO4��Һ��NH4Cl��Һ���ش��������⣺
��1����ȡ5mL������Һ���ֱ��ˮϡ����50mL��pH�ϴ����________��Һ
��2����ȡ5mL������Һ���ֱ���ȣ��¶���ͬ����pH��С����________��Һ
��3��H2SO4��Һ��NH4Cl��Һ����ˮ�������c(H+)֮��Ϊ__________
��4��ȡ5mL NH4Cl��Һ����ˮϡ����50mL��c(H+) ____________ 10-6mol·L-1���>������<����=������c(NH4+)��c(H+)_______________�����������С�����䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ�У���Ũ�ȹ�ϵ��ȷ����
A�������£�pH=6���ɴ������������ɵĻ����Һ�У�c(Na+)>c(CH3COO-)
B. ��Cl2ͨ�����KOH��Һ�У�c(ClO-)+c(Cl-)=c(K+)
C. 0.1mol·L-1��Na2S��Һ�У�c(OH-)= c(H+)+c(HS-)+2 c(H2S)
D�������£�pH=2��������pH=12�İ�ˮ�������ϣ�������Һ�У�
c(Cl-)> c(H+)> c(NH4+)> c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��W��R��5�ֶ�����Ԫ�أ���ԭ��������������X�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�������������Ǵ�����������3����Z��W��R����ͬһ���ڣ�R��Y����ͬһ�壬Z��Wԭ�ӵĺ��������֮����Y��Rԭ�ӵĺ��������֮����ȡ�����˵����ȷ��������)��
A.Ԫ��Y��Z��W������ͬ���Ӳ�ṹ�����ӣ���뾶��������
B.Ԫ��X������Ԫ��Y�γɻ�����X2Y2
C.Ԫ��Y��R�ֱ���Ԫ��X�γɵĻ���������ȶ��ԣ�XmY��XmR
D.Ԫ��W��R������������ˮ���ﶼ��ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ��֤�����������Է����еķ�Ӧ���Ƿ��ȷ�Ӧ���Դ�˵����������ȷ����(����)
A�����еķ��ȷ�Ӧ�����Է����е�
B�����е��Է���Ӧ���Ƿ��ȵ�
C���ʱ���Ӱ�췴Ӧ�Ƿ�����Է��Ե�һ����Ҫ����
D���ʱ��Ǿ�����Ӧ�Ƿ�����Է��Ե�Ψһ�о�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com