
据新浪科技网报道:美国科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可能是21世纪人类最伟大的发现之一,将有望解决未来人类的能源危机。无线电频率可以降低盐水中所含元素之间的结合力,释放出氢原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述“结合力”的实质是( )
A.离子键 B.共价键
C.一种静电引力 D.一种静电斥力
科目:高中化学 来源: 题型:
下列化学用语表示正确的是( )
①甲基的电子式: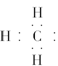
②乙炔的最简式:C2H2
③蔗糖的分子式:C12H22O11
④乙醛的结构简式:CH3COH
⑤苯分子的比例模型: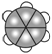
A.①②④ B.③⑤
C.②③⑤ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学变化的是 ( )
①对空气进行降温加压 ②金刚石变成石墨 ③NaCl熔化 ④碘溶于CCl4中 ⑤HCl溶于水电离出H+和Cl- ⑥电解熔融的Al2O3制取Al
A.②③⑤ B.②⑤⑥
C.②⑥ D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)过氧化钠的电子式: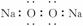 (×)
(×)
(2014·江苏,2A)
(2)氢氧根离子的电子式: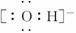 (√)
(√)
(2013·江苏,2B)
(3)NH4Br的电子式: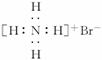 (×)
(×)
(2012·海南,9A)
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的四种短周期元素。X与W可形成四面体形的共价化合物,该化合物常用作灭火剂。Y的次外层电子数等于其最外层和最内层电子数之和的2倍,Y、Z的最外层电子数之和等于W的最外层电子数。
(1)用化学符号表示X的一种核素_____________________________________________。
(2)写出Y的单质与X的最高价氧化物反应的化学方程式_________________________。
(3)Z的单质在W的单质中燃烧,生成的产物中各原子的最外层均达到8电子稳定结构的分子为________。
(4)用电子式表示Y与W形成化合物的过程为_____________。
(5)XW4的电子式为____________________________________________________。
(6)W的氢化物R是实验室一种常用试剂的主要成分,该试剂可用于实验室多种气体的制备,写出实验室制取气体时满足下列条件的离子方程式。
①R作氧化剂:__________________________________________________。
②R作还原剂:_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g)2SO3(g),ΔH<0的正、逆反应速率的影响如图所示:
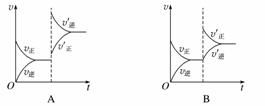
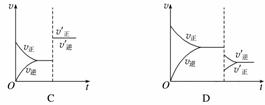
(1)加催化剂对反应速率影响的图像是________(填序号,下同),平衡________移动。
(2)升高温度对反应速率影响的图像是__________,平衡向________方向移动。
(3)增大反应容器体积对反应速率影响的图像是________,平衡向________方向移动。
(4)增大O2的浓度对反应速率影响的图像是__________,平衡向________方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烷(C3H8)和丙烯(C3H6)都可作火炬燃料。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)=CH4(g)+HC
 CH(g)+H2(g) △H1=+156.6 kJ·mol-1
CH(g)+H2(g) △H1=+156.6 kJ·mol-1
CH3CH
 CH2(g)=CH4(g)+HC
CH2(g)=CH4(g)+HC
 CH(g ) △H2=+32.4 kJ·mol-1
CH(g ) △H2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)=CH3CH
 CH2(g)+H2(g) 的△H= kJ·mol-1。
CH2(g)+H2(g) 的△H= kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池负极反应式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中:
①c(OH-)= 。
②c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com