
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
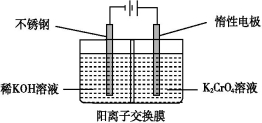
下列说法不正确的是
A.在阴极室,发生的电极反应为:2H2O+2e- 2OH-+H2↑
2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+ Cr2O72-+H2O向右移动
Cr2O72-+H2O向右移动
C.该制备过程中总反应的化学方程式为4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr)为d,则此时铬酸钾的转化率为1-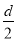
D
【解析】
试题分析:A、根据装置图可知,左侧是阴极室,阴极是氢离子放电,腐蚀还原反应生成氢气,正确;B、阳极发生氧化反应,氢氧根离子放电生成氧气,导致阳极区氢离子浓度增大,2CrO42-+2H+ Cr2O72-+H2O向右移动,正确;C、电解时,铬酸钾和水放电生成重铬酸钾、氢气、氧气和氢氧化钠,所以总反应的化学方程式为4K2CrO4+4H2O
Cr2O72-+H2O向右移动,正确;C、电解时,铬酸钾和水放电生成重铬酸钾、氢气、氧气和氢氧化钠,所以总反应的化学方程式为4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑,正确;D、设加入反应容器内的K2CrO4为1mol,则n(K)=2mol, n(Cr)=1mol,反应过程中有xmol K2CrO4转化为K2Cr2O7,由于阴极是氢离子放电,造成阴极区氢氧根离子增多,所以K+向阴极区移动,补充氢离子,根据化学方程式可知,xmol K2CrO4转化为K2Cr2O7,则阴极区生成KOH的物质的量是xmol,则阳极区剩余n(K)=(2-x)mol,Cr元素不变,仍是1mol,根据:K与Cr的物质的量之比为d,解得(2-x)/1=d,x=2-d,转化率为(2-d)/1×100%=2-d,错误,答案选D。
2K2Cr2O7+4KOH+2H2↑+O2↑,正确;D、设加入反应容器内的K2CrO4为1mol,则n(K)=2mol, n(Cr)=1mol,反应过程中有xmol K2CrO4转化为K2Cr2O7,由于阴极是氢离子放电,造成阴极区氢氧根离子增多,所以K+向阴极区移动,补充氢离子,根据化学方程式可知,xmol K2CrO4转化为K2Cr2O7,则阴极区生成KOH的物质的量是xmol,则阳极区剩余n(K)=(2-x)mol,Cr元素不变,仍是1mol,根据:K与Cr的物质的量之比为d,解得(2-x)/1=d,x=2-d,转化率为(2-d)/1×100%=2-d,错误,答案选D。
考点:考查电解池的反应原理的应用


科目:高中化学 来源:2014-2015安徽省高二上学期第一次质量检测化学试卷(解析版) 题型:选择题
某蓄电池放电、充电时的反应为Fe+Ni2O3+3H2O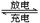 Fe(OH)2+2Ni(OH)2
Fe(OH)2+2Ni(OH)2
下列推断中正确的是
①放电时,Fe为正极,Ni2O3为负极
②充电时,阴极上的电极反应式是:Fe(OH)2+2e-===Fe+2OH-
③充电时,Ni(OH)2为阳极
④该蓄电池的电极必须是浸在某
种碱性电解质溶液中
A.①②③ B.①②④ C.①③④ D.②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市三校高一上学期期中化学试卷(解析版) 题型:选择题
下列说法错误的是
A.向粗盐溶液中滴加盐酸和BaCl2溶液,产生白色沉淀,则说明粗盐中含有SO42-
B.向精盐溶液中滴加盐酸和BaCl2溶液,无明显现象,则说明精盐中不含SO42-
C.向蒸馏水中滴加稀HNO3和AgNO3溶液,产生白色沉淀,则说明蒸馏水中含有Cl-
D.向自来水中滴加稀HNO3和AgNO3溶液,产生白色沉淀,则说明自来水中含有Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市三校高一上学期期中化学试卷(解析版) 题型:选择题
下列有关物理量相应的单位表达中,错误的是
A.摩尔质量g/mol B.气体摩尔体积L/g
C.物质的量浓度mol/L D.物质的量 mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高二10月月考化学试卷(解析版) 题型:选择题
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是
A.向水中投入一小块金属钠
B.将水加热煮沸
C.向水中通入二氧化碳气体
D.向水中加食盐晶体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高二10月月考化学试卷(解析版) 题型:选择题
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型,NiMH中的M表示储氢金属或合金,该电池在充电过程中的总反应方程式是Ni(OH)2+M===NiOOH+MH。
已知:6NiOOH+NH3+H2O+OH-===6Ni(OH)2+NO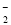
下列说法正确的是
A.NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-===Ni(OH)2+OH-
B.充电过程中OH-从阳极向阴极迁移
C.充电过程中阴极的电极反应式:H2O+M+e-===MH+OH-,H2O中的H被M还原
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高二10月月考化学试卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其他电极均为Cu,则
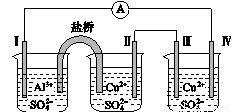
A.电流方向:电极Ⅳ →  → 电极Ⅰ
→ 电极Ⅰ
B.电极Ⅰ发生还原反应
C.电极Ⅱ逐渐溶解
D.电极Ⅲ的电极反应:Cu2++2e-===Cu
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高一10月月考化学试卷(解析版) 题型:选择题
用10 mL 0.1 mol/L的BaCl2溶液可分别使相同体积的Fe2(SO4)3、ZnSO4和K2SO4三种溶液中的SO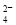 完全转化为BaSO4沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
完全转化为BaSO4沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
A.3∶2∶2 B.1∶2∶3 C.1∶3∶3 D.3∶1∶1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江安达市高二第一次月考试卷化学试卷(解析版) 题型:选择题
水的电离过程为H2O H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( )
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14, K(35℃)=2.1×10-14。则下列叙述正确的是( )
A.c(H+)随着温度升高而降低 B.35℃时,c(H+)>c(OH-)
C.水的电离度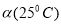 >
>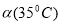 D.水的电离是吸热的
D.水的电离是吸热的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com