
| A. | 将地沟油回收加工成燃料,可提高资源的利用率 | |
| B. | 把蔬菜或海产品用福尔马林浸泡,可保鲜并消毒 | |
| C. | 推广使用聚碳酸酯等可降解塑料,可减少白色污染 | |
| D. | 化石燃料的蕴藏量有限且不可再生,最终将会枯竭 |
分析 A.地沟油对人体有害,将地沟油回收加工成燃料,可充分利用资源;
B.福尔马林对人体有害;
C.聚碳酸酯可降解;
D.化石燃料不可再生.
解答 解:A.地沟油对人体有害,将地沟油回收加工成燃料,可充分利用资源,故A正确;
B.福尔马林对人体有害,不能用于食品的浸泡,故B错误;
C.聚碳酸酯可降解,可减少污染,故C正确;
D.天然气、煤、石油属于化石燃料.在我国能源领域占有重要的地位.化石燃料燃烧无论充分燃烧还是不充分燃烧都会对环境产生影响,且储量有限,是一种有局限性的能源,故D正确.
故选B.
点评 本题综合考查化学环境的污染与保护,侧重于化学与生活、环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:选择题
| A. | 14g乙烯和丙烯的混合物中总原子数为3NA个 | |
| B. | 2mol/L的硫酸溶液中含有的H+离子数为4NA | |
| C. | 1mol 氯气与足量的铁反应后转移的电子数为3NA | |
| D. | 密闭容器中1molN2与3molH2在铂催化下充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数 | B. | 中子数 | C. | 电子数 | D. | 质量数 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 钠投入到水中 2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 氯化铵溶液与浓NaOH溶液加热 NH4++OH-═NH3•H2O | |
| C. | 氯化铝溶液中滴入过量氨水 Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 铁片插入氯化铁溶液中 Fe+Fe3+═2Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
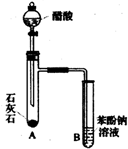 有机化合物分子中的基团之间存在着相互影响.
有机化合物分子中的基团之间存在着相互影响.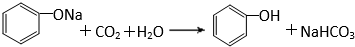 .
. 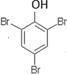 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO+H2O═Ca(OH)2 | B. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+CO2 | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | Ca(ClO)2+2HCl═CaCl2+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

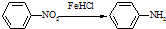 (苯胺,易被氧化)
(苯胺,易被氧化)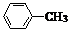 .
.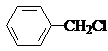 .
.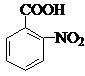 .反应②③两步能否互换不能,(填“能”或“不能”)理
.反应②③两步能否互换不能,(填“能”或“不能”)理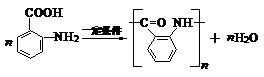 ;反应⑤的化学方程式是
;反应⑤的化学方程式是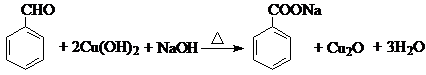 .
.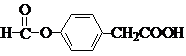 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3•H2O | 1.8×10-5 |
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1×10-10 |
| BaCO3 | 2.6×10-9 |
| CaSO4 | 7×10-5 |
| CaCO3 | 5×10-9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com