
| A、是否为大量分子或离子的集合体 |
| B、分散质微粒的大小不同 |
| C、能否通过滤纸或半透膜 |
| D、是否均一、稳定、透明 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
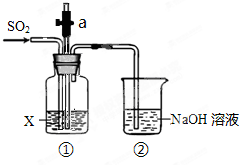 某同学用如图所示装置探究SO2的性质.
某同学用如图所示装置探究SO2的性质.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 L 1 mol/L的NaClO 溶液中含有ClO-的数目为NA |
| B、78 g 苯含有C=C 双键的数目为3NA |
| C、常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA |
| D、标准状况下,6.72 L 氯气与水充分反应转移的电子数目为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液的物质的量浓度为1mol/L |
| B、该溶液中含有35.5g Na2SO4 |
| C、配制1 00ml该溶液需用7.1g Na2SO4 |
| D、量取100ml该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铝溶液中滴加过量浓氨水:Al3++4OH-═AlO2-+2H2O |
| B、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
| C、碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O |
| D、过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在熔化状态下能导电的化合物为离子化合物 |
| B、根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸 |
| C、CO2、SiO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2为碱性氧化物 |
| D、因为Na2O的水溶液能导电,所以Na2O是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
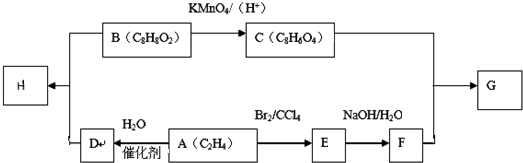
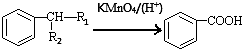 (-R1、-R2表示氢原子或烃基)
(-R1、-R2表示氢原子或烃基)查看答案和解析>>
科目:高中化学 来源: 题型:
 金属钠和过氧化钠分别与水反应有很多值得探究的问题.
金属钠和过氧化钠分别与水反应有很多值得探究的问题.| 实验操作 | 预期的实验现象和结论 |
| 实验操作 | 预期的实验现象和结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com