
�����±��ṩ��������ҩƷ���ܴﵽ��Ӧʵ��Ŀ�ĵ���
��� | �� �� | ҩ Ʒ | ʵ �� Ŀ �� |
A | ������ƽ(������)��Ͳ�ձ�ҩ�ײ����� | NaCl��������ˮ | ����һ�����ʵ���Ũ�ȵ�NaCl��Һ |
B | �ձ�������ʯ�����ƾ���©������̨(����Ȧ������) | �ֱ���������ˮ | �ֱ�������ᴿ |
C | ������ƿ�¶ȼ�������β�ӹ���ƿ����̨(����Ȧ������) | ��������������������� | �ᴿ��������������������� |
D | ���ֹ���ձ���Ͳ���β����������ĭ���ϰ�ֽ�� | 0.5mol��L-1����0.55mol��L-1NaOH | �кͷ�Ӧ��Ӧ�ȵIJⶨ |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ����ᡢ����������أ������й�˵������ȷ����
A��ȼú�м���CaO��ɼ�������������ŷ���
B�����ࡢ��֬�������ʶ���������Ҫ��Ӫ�����ʣ���������Ȼ�߷��ӻ�����
C��Ư�ۡ�����������������ˮ�������仯ѧԭ����ͬ
D����ȫ��ÿ�걻��ʴ�Ľ����У��绯ѧ��ʴ�Ȼ�ѧ��ʴ��ռ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������к�ƽ�������ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���У�����ȷ����
A��H��D��T��Ϊͬλ��
B��NaHCO3��HCOONa���������Ӽ����ۼ�
C�����³�ѹ�£�22.4 L CCl4����NA��CCl4����
D�������£�23 g NO2����NA����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и�������������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��ӦX(g)��Y(g) R(g)��Q(g)��ƽ�ⳣ�����¶ȵĹ�ϵ���±���830��ʱ����һ��2 L���ܱ������г���0.2 mol X��0.8 mol Y����Ӧ��ʼ4 s��
R(g)��Q(g)��ƽ�ⳣ�����¶ȵĹ�ϵ���±���830��ʱ����һ��2 L���ܱ������г���0.2 mol X��0.8 mol Y����Ӧ��ʼ4 s��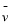 (X)��0.005 mol/(L��s)������˵����ȷ����
(X)��0.005 mol/(L��s)������˵����ȷ����
�¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A��4 sʱ������c(Y)��0.76 mol/L
B��830���ƽ��ʱ��X��ת����Ϊ80%
C����Ӧ��ƽ��������¶ȣ�ƽ�������ƶ�
D��1200��ʱ��ӦR(g)��Q(g) X(g)��Y(g)��ƽ�ⳣ��K��0.4
X(g)��Y(g)��ƽ�ⳣ��K��0.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����еڶ�������Բ��Ի�ѧ�Ծ��������棩 ���ͣ������
(14��)��Ȼ����һ����Ҫ�������Դ�ͻ���ԭ�ϣ�����Ҫ�ɷ�Ϊ������ͼΪ����Ȼ��Ϊԭ���Ʊ�������Ʒ�Ĺ�������
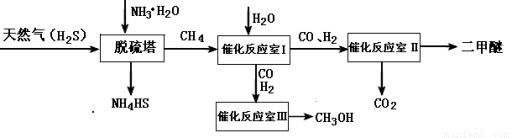
��1��CH4��VSEPRģ��Ϊ
��2��һ����������NH4HS��Һ��ͨ��������õ���������ʹ��ˮ������д����ˮ����ʱ�Ļ�ѧ��Ӧ����ʽ
��3��ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2(g)+CO(g)  CH3OH(g)����H=-90.8 kJ��mol1
CH3OH(g)����H=-90.8 kJ��mol1
��2CH3OH(g)  CH3OCH3(g)+H2O(g)����H=-23.5kJ��mol1
CH3OCH3(g)+H2O(g)����H=-23.5kJ��mol1
��CO(g)+H2O(g)  CO2(g) + H2(g)����H=-41.3 kJ��mol1
CO2(g) + H2(g)����H=-41.3 kJ��mol1
�����Ӧ���ҵ��Ȼ�ѧ����ʽΪ
��4����һ�������£���Ӧ�Ң�(�ݻ�ΪVL)�г���amolCO��2amolH2 ���ڴ��������·�Ӧ���ɼ״���
CO(g) +2H2(g) CH3OH(g)��CO��ƽ��ת�������¶�ѹǿ�Ĺ�ϵ��ͼ��ʾ����P1 P2(�<����=����>��)��
CH3OH(g)��CO��ƽ��ת�������¶�ѹǿ�Ĺ�ϵ��ͼ��ʾ����P1 P2(�<����=����>��)��
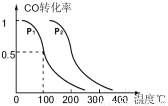
���������������������£���Ӧ�Ң�������a mol CO��2a mol H2���ﵽ��ƽ��ʱ��CO��ת���� (�������С�����䡱)��
����P1ѹǿ�£�100��ʱ����Ӧ��CH3OH(g) CO(g)+2H2(g)��ƽ�ⳣ��Ϊ (�ú�aV�Ĵ���ʽ��ʾ)
CO(g)+2H2(g)��ƽ�ⳣ��Ϊ (�ú�aV�Ĵ���ʽ��ʾ)
��5����ѧ���õ����ز�����ͭ��װ��ͼ���˹����ϵͳ�����ø�װ�óɹ���ʵ������CO2��H2O�ϳ�CH4ͭ�缫����ĵ缫��Ӧʽ

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����еڶ�������Բ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ������������������������˵������ȷ����
A��ʳ�����ڳ�ȥůˮƿ�е�ˮ��
B��14C��������������������14C��12C��Ϊͬ��������
C��������ά�غ���֬��������Ȼ�߷��ӻ�����
D��pH��5.6~7.0֮��Ľ�ˮͨ����Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ���������������ѧ���������п��ԣ���ģ����ѧ�Ծ��������棩 ���ͣ������
�����12�֣�TiCl4��һ����Ҫ�Ļ���ԭ�ϣ��乤ҵ�����������£�
2FeTiO3(s) + 7Cl2(g) + 6C (s) 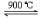 2TiCl4 (g) + 2FeCl3(g) + 6CO(g) �C Q (Q>0)
2TiCl4 (g) + 2FeCl3(g) + 6CO(g) �C Q (Q>0)
�ش��������⣺
1.�÷�Ӧ�ﵽƽ�����ʹ����Ӧ��������ɲ�ȡ�ķ�����_________����ѡ���ţ�
a.��ѹ b.����̼ c.���� d.��ʱ����CO
2.��������Ӧ�ڹ̶�������ܱ������з�����һ����˵����Ӧ�Ѵ�ƽ�����_______��(ѡ���ţ�
a. ��Ӧ�ﲻ��ת��Ϊ������
b. ¯��FeTiO3��TiCl4 �������ȱ��ֲ���
c. ��Ӧ����ЧӦ���ٸı�
d. ��λʱ���ڣ�n(FeTiO3)���ģ�n(FeCl3������=1:1
3.������Ӧ�����зǽ���Ԫ��ԭ�ӵİ뾶�Ӵ�С��˳��Ϊ_____________�����в�����ͬ�����ֲ��������������Ԫ���γ�_____���ӣ�����ԡ��Ǽ��ԡ�����ͨ���Ƚ�____________�����ж�������Ԫ�صķǽ����ԡ�
4.������Ӧ�У��ǽ�����������Ԫ��ԭ�ӵĵ��ӹ�ռ��_______��ԭ�ӹ�������������Ų�ʽΪ____________�����γɵĹ�̬������ֻ��һ��ǿ�ҵ������������õ�������______���塣
5.Ϊ��������������ҵ��TiCl4�����Ժ��ȼ��������������CO�ɺϳɼ״�������������ʧ���������������ڳ�����ø��ָ���Ʒ��ǰ���£��ϳ�192 kg�״��������貹��H2 mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ���������������ѧ���������п��ԣ���ģ����ѧ�Ծ��������棩 ���ͣ�ѡ����
������ʵ����Ԫ�������ɽ��͵���
A���е㣺H2O>H2Se>H2S B�����ԣ�H2SO4>H2CO3>HClO
C��Ӳ�ȣ�I2>Br2>Cl2 D�����ԣ�KOH>NaOH>Al(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и���������⣨�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���н���ʵ����ʵ�ķ���ʽ��ȷ����
A�����������ڿ����б�������4Fe2����3O2��6H2O��4Fe��OH��3
B����CH2Br-COOH�м�������������������Һ�����ȣ�CH2Br-COOH+OH�� CH2Br-COO��+ H2O
CH2Br-COO��+ H2O
C��FeCl3��Һ��ͨ��SO2����Һ��ɫ��ȥ��2Fe3++SO2 +2H2O = 2Fe2+ + SO42��+ 4H+
D��̼������Һ�����̪��죺CO32��+ 2H2O  H2CO3 + 2OH��
H2CO3 + 2OH��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com