

| A. | 2SO3(g)?2SO2(g)+O2(g)△H>0 | B. | N2(g)+3H2(g)?2NH3(g)△H<0 | ||
| C. | 4NH3(g)+5O2(g)?4NO+6H2O(g)△H<0 | D. | H2(g)+CO(g)?C(s)+H2O(g)△H>0 |
分析 由图甲可知,T2先达到平衡,则T2<T1,温度高生成物的浓度大,则该反应为吸热反应;
由图乙可知,增大压强,逆反应速率大于正反应速率,则加压平衡逆向移动,可知该反应中气体的化学计量数之和反应前<反应后,以此来解答.
解答 解:由图甲可知,T2先达到平衡,则T2<T1,温度高生成物的浓度大,则该反应为吸热反应;
由图乙可知,增大压强,逆反应速率大于正反应速率,则加压平衡逆向移动,可知该反应中气体的化学计量数之和反应前<反应后,则
A.为吸热反应,且2<2+1,符合题意,故选;
B.为放热反应,故B不选;
C.为放热反应,故C不选;
D.1+1>1,不符合题意,故D不选;
故选A.
点评 本题考查化学平衡的影响因素及平衡图象,为高频考点,把握平衡及速率的影响因素等为解答的关键,侧重分析与应用能力的考查,注意温度、压强对反应的影响,题目难度不大.


科目:高中化学 来源: 题型:解答题
 酚醛树脂(phenolic resin)是人类合成的第一种高分子材料,至今仍被广泛使用.某校化学兴趣小组的同学通过下列方法在实验室制备酚醛树脂:
酚醛树脂(phenolic resin)是人类合成的第一种高分子材料,至今仍被广泛使用.某校化学兴趣小组的同学通过下列方法在实验室制备酚醛树脂: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽车尾气中有毒的NO和CO气体经充分反应后,理论上可完全转化为N2和CO2 | |
| B. | 使用高效催化剂可有效增大正反应速率 | |
| C. | 反应达到平衡后,NO的反应速率保持恒定 | |
| D. | 单位时间内CO和CO2减少的物质的量相等时,反应达到平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;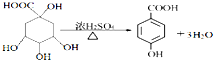 _,反应类型是消去反应;
_,反应类型是消去反应; (其中任一种);(任写一种)
(其中任一种);(任写一种) .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饮用水越纯净对人体越有益 | |
| B. | 调味剂和营养剂加得越多越好 | |
| C. | 垃圾分类有利于资源回收利用,废易拉罐不是有害垃圾,可回收利用 | |
| D. | 为消除碘缺乏症,卫生部规定必须在食盐中加碘单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
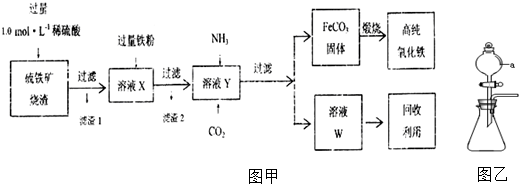
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ②③④⑥ | C. | ①④⑤⑥ | D. | ②⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com