
| A、加入20g固体NaOH,搅拌、溶解 |
| B、将溶液加热浓缩至0.2L |
| C、加入10mol/L的NaOH溶液0.1L,再稀释至1.5L |
| D、加入1L 1.5mol/L的NaOH溶液混合均匀 |
| 1L |
| 0.2L |
| n |
| V |
| 1L |
| 0.2L |
| 0.5mol/L×1L+10mol/L×0.1L |
| 1.5L |


科目:高中化学 来源: 题型:
| A、1:1 | B、1:2 |
| C、2:3 | D、3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于1.0g?cm-3 |
| B、小于0.8g?cm-3 |
| C、介于0.8~1.0g?cm-3之间 |
| D、不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
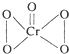 ,据此推断该氧化物( )
,据此推断该氧化物( )| A、稳定性比较高,不易分解 |
| B、稳定性比较低,易分解 |
| C、分子中所有原子均达到8电子稳定结构 |
| D、属于碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、42.1% |
| B、43.1% |
| C、44.1% |
| D、45.1% |
查看答案和解析>>
科目:高中化学 来源: 题型:
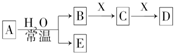 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断不正确的是( )
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断不正确的是( )| A、若A是单质,B和D的反应是OH-+HCO3-═H2O+CO32-,则E是一种清洁能源 |
| B、若D为CO,C能和E反应,则A一定为Na2O2 |
| C、若X是Na2CO3,C为含极性键的分子,则A一定是氯气,且D和E能发生反应 |
| D、若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在医疗上,碳酸氢钠是治疗胃酸过多症的一种药剂 |
| B、工业上生产漂粉精,是通过氯气与石灰水作用制成的 |
| C、高性能通信材料光导纤维的主要原料是二氧化硅 |
| D、空气中的NO2是造成光化学烟雾的主要因素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
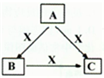 A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(其它产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(其它产物已略去),下列说法错误的是( )| A、若X为O2,则A可为硫化氢 |
| B、若X为KOH溶液,则A可能为AlCl3 |
| C、若X为Fe,则C可能为Fe(NO3)2 |
| D、若A、B、C均为焰色反应呈黄色的化合物,则X可能为Na |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com