
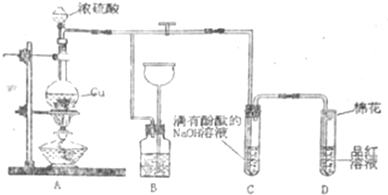
分析 浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,反应生成的SO2具有酸性和还原性,可用排饱和NaHSO3溶液收集,具有漂白性,可使品红溶液褪色,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,结合题目要求解答该题,
(1)浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应生成硫酸铜、二氧化硫和水;
(2)SO2易溶于水,具有酸性和还原性;
(3)SO2溶液具有酸性,可与NaOH溶液反应,具有漂白性,可使品红溶液褪色;
(4)二氧化硫有毒,不能排放到空气中,应可氢氧化钠溶液反应;
(5)①观察稀硫酸溶液呈无色,可说明SO42-无色;
②观察CuSO4粉末呈白色,不能证明蓝色只与Cu2+有关;
③稀释CuSO4溶液,溶液蓝色变浅,因阳离子和阴离子浓度都变浅,不能证明;
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色,铜离子浓度减小,可说明与铜离子有关;
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色,铜离子物质的量不变,可说明与铜离子有关,
(6)浓硫酸具有强氧化性,而稀硫酸与铜不反应,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,则反应后溶液中一定含有硫酸,浓硫酸与铜反应的过程中,浓度会变稀,而稀硫酸不与铜反应,所以会有剩余,加入硝酸钾后,硝酸根离子在氢离子存在情况下有强氧化性,能与铜反应,剩余硫酸浓度为amol/L,依据氧化还原反应单质转移守恒计算得到.
解答 解:(1)浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)SO2易溶于水,具有酸性和还原性,可与酸性KMnO4、Na2SO3溶液反应,难溶于水饱和的NaHSO3溶液,可用排饱和NaHSO3溶液收集,
故答案为:④;
(3)SO2溶液具有酸性,可与NaOH溶液反应,发生:SO2+2OH-=SO32-+H2O,则滴加酚酞的氢氧化钠溶液褪色,具有漂白性,可使品红溶液褪色,
故答案为:溶液具有酸性,中和了溶液中的NaOH;漂白性;
(4)二氧化硫有毒,不能排放到空气中,应可氢氧化钠溶液反应,则棉花上可浸有氢氧化钠溶液,防止污染空气,
故答案为:吸收多余的二氧化硫,防止污染空气;
(5)①观察稀硫酸溶液呈无色,可说明SO42-无色;
②观察CuSO4粉末呈白色,不能证明蓝色只与Cu2+有关;
③稀释CuSO4溶液,溶液蓝色变浅,因阳离子和阴离子浓度都变浅,不能证明;
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色,铜离子浓度减小,可说明与铜离子有关;
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色,铜离子物质的量不变,可说明与铜离子有关,
则对实验目的没有意义的是②③,
故答案为:②③;
(6)浓硫酸具有强氧化性,而稀硫酸与铜不反应,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,则反应后溶液中一定含有硫酸,浓H2SO4与铜反应的过程中,浓度会变稀,而稀硫酸不与铜反应,所以会有剩余,加入硝酸钾后,硝酸根离子在氢离子存在情况下有强氧化性,能与铜反应,剩余硫酸浓度为amol/L,则硫酸物质的量=0.0125L×amol/L=0.0125amol,n(Cu)=$\frac{7.2g}{64g/mol}$=0.1125mol,n(H2SO4)=0.0125L×18mol/L=0.225mol,参加反应的硫酸物质的量=0.225mol-0.0125amol,Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,2mol硫酸反应单质转移2mol,则电子转移为:0.225mol-0.0125amol,设加入硝酸钾物质的量为x,依据电子守恒列式计算得到:0.1125mol×2=0.225mol-0.0125amol+3x,得到x=$\frac{a}{240}$mol,
故答案为:反应过程中浓H2SO4被不断消耗,生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应;$\frac{a}{240}$;
点评 本题综合考查性实验设计、电子转移守恒的计算,侧重于学生的分析能力和实验能力的考查,为高考常见题型,题目难度中等,注意把握相关物质的性质以及实验原理.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 950mL,111.2g | B. | 500mL,117g | C. | 1000mL,l17g | D. | 任意规格,117g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀醋酸与氢氧化钠溶液的反应:H++OH-=H2O | |
| B. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| C. | 氯气与氯化亚铁溶液的反应:Cl2+2Fe2+=2Cl-+2Fe3+ | |
| D. | 碳酸钙溶液与足量稀盐酸的反应:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧 | |
| C. | 处理废水时加入明矾作为消毒剂对水进行杀菌消毒 | |
| D. | 某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com