
| A. | N5+中氮-氮之间是以共价键结合 | B. | N5+具有35个电子 | ||
| C. | 化合物N5AsF6中As的化合价为+5 | D. | 化合物N5AsF6中F的化合价为-1 |
分析 A.非金属元素之间易形成共价键;
B.阳离子电子数=质子数-电荷数;
C.N5AsF6中阳离子是N5+,则阴离子是AsF6-,AsF6-中F元素显-1价;
D.氟元素是最活泼的非金属元素,F原子最外层有7个电子,容易得1个电子变成8电子稳定结构.
解答 解:A.非金属元素之间易形成共价键,N5+中氮-氮之间是以共价键结合,故A正确;
B.阳离子电子数=质子数-电荷数=5×7-1=34,故B错误;
C.N5AsF6中阳离子是N5+,则阴离子是AsF6-,AsF6-中F元素显-1价,所以As元素显+5价,故C正确;
D.氟元素是最活泼的非金属元素,F原子最外层有7个电子,容易得1个电子变成8电子稳定结构,所以该化合物中F元素为-1价,故D正确;
故选B.
点评 本题考查化学键、电子数的计算、化合价判断等知识点,侧重考查学生分析计算能力,明确化学键概念、电子数的计算方法及化合价判断方法即可解答,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | KClO3在反应中是氧化剂 | |
| B. | 1mol KClO3参加反应,在标准状况下能得到22.4L气体 | |
| C. | 在反应中H2C2O4既不是氧化剂也不是还原剂 | |
| D. | 1mol KClO3参加反应有1mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
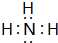 ;B的水溶液不呈中性的原因NH4++H2O?NH3.H2O+H+(用离子方程式表示)
;B的水溶液不呈中性的原因NH4++H2O?NH3.H2O+H+(用离子方程式表示)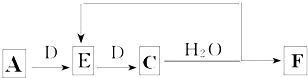
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省哈尔滨市高三上学期期中考试化学试卷(解析版) 题型:选择题
一定条件下存在反应:CO(g)+H2O(g) CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1molH2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1molH2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
A.容器I、II中正反应速率相同
B.容器I、III中反应的平衡常数相同
C.容器I中CO的物质的量比容器II中的少
D.容器I中CO的转化率与容器II中CO2的转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
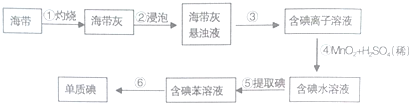
| A. | 步骤①④⑤均属于化学变化 | |
| B. | 步骤④中MnO2的作用是催化剂 | |
| C. | 步骤⑤所用主要仪器是分液漏斗、烧杯 | |
| D. | 步骤⑥操作名称是萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
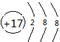 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 7种 | C. | 6种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
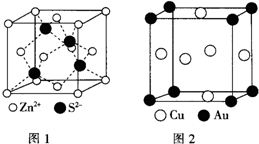
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 G在周期表的第七列 |
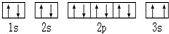 ,该同学所画的电子排布图违背了泡利不相容原理
,该同学所画的电子排布图违背了泡利不相容原理查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| A | SO2(乙炔) | 溴水 | 洗气 |
| B | 苯(溴) | KI溶液 | 分液 |
| C | 乙醇(乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| D | 乙烷(乙烯) | KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com