
����Ŀ�����������ѳ�Ϊ���ͬ��ע�Ļ��⣬ȼú����������β���г����е�NOx��SO2��H2S����Ⱦ������γ����꣬�ƻ����������ۺ������ǵ�ǰ��Ҫ���о����⡣
���������Ƕ���������������ۣ����в���ȷ����__________
a��ɱ��ˮ�еĸ��������������ʳ�����Դ���ƻ�ˮ����̬ϵͳ
b���Ե��ߡ����졢���������ݵȾ������������
c�����³�����ն�
d��������̼�Ĺ����ŷţ����γ��������Ҫԭ��֮һ
������ⷨ����������������нϸߵĻ���Ч��;���Ч�棨ͼ�е缫��Ϊʯī����

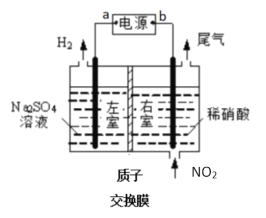
��1�����NO�Ʊ�NH4NO3ԭ�����Ϸ���ͼ��ʾ��
������Ϊʯī_____(��1��2)���õ缫�ķ�ӦʽΪ_____________��
��Ϊʹ���ĸ�����Ҳ��ȫת��ΪNH4NO3����Ҫ���������X�Ļ�ѧʽΪ___________��
��2�����Ϸ���ͼװ�ý���ģ����NO2����ʵ�飬�ɻ������ᡣ
����ӵ�Դa��Ϊ______�������ҷ����ĵ缫��ӦʽΪ_____________��
�����б�״����2.24L NO2�����գ�ͨ�����ӽ���Ĥ(ֻ��������ͨ��)��H+Ϊ______mol��
���ú�NO��NO2(������NO2ת��ΪN2O4)�ķ�������ģ���ⷨ����ʵ�顣�������У��в���NOת��ΪHNO2��ʵ�����ʱ�����������Һ��������1 mol HNO3��0.1 mol HNO2��ͬʱ�����ռ�����״����28L H2��ԭ������NO��NO2�������Ϊ____________��
���𰸡�cd 2 NO-3e-+2H2O=NO3-+4H+ NH3 �� 2H++2e- = H2������2H2O+2e- = H2��+2OH-�� 0.1 8��3
��������
I.������������ʽ����жϣ�
��.(1)���NO�Ʊ�NH4NO3ʱ������������NOʧ���ӵ�������Ӧ������������NO�õ��ӵĻ�ԭ��Ӧ�����ݵ缫��Ӧ�ж���Ҫ���������X��
(2)�ٸ���ͼ֪�����ʱ�������е缫�������ӷŵ�����������������Ϊ�����ң�����Ϊ�����ң�������ͨ����ǵ���������ɵ������ᣬ���������ϵ�������ʧ���Ӻ�ˮ���������n(NO2)=0.1mol��������ӦʽΪNO2-e-+H2O=NO3-+2H+����0.2mol���������ɣ���Ϊ��0.1mol�������ɣ��ݴ˷����жϣ��۸����������������ת�Ƶĵ�����������������1mol HNO3��0.1molHNO2���ɣ���������������������ת�Ƶĵ��ӵ����ʵ������ٽ��Nԭ���غ㼰ת�Ƶ����غ���ʽ���㡣
��a�������к����ᡢ���ᣬ������н�ǿ�����ԣ����е��������ǿ�����ԣ���ɱ��ˮ�еĸ��������������ʳ�����Դ���ƻ�ˮ����̬ϵͳ����a��ȷ��b��������н�ǿ�����ԣ����е��������ǿ�����ԣ����ߡ������к��н���ͭ�����ȣ������������к��н��������Σ����Ƕ��ܺ������еijɷַ�Ӧ����b��ȷ��c�����³�����ն����Ƿ��������������꣬��c����d.������������������Ĺ����ŷ����γ��������Ҫԭ������̼�����γ������ԭ��d����ѡcd��
��(1)�ٸ���ͼʾ�����ʱ�������е缫��NO�ŵ�����NH4+���缫��ӦʽΪNO+5e-+6H+=NH4++H2O��������Ϊ�����ң�����Ϊ�����ң�������ͨ���NO������������������ӣ�����ʯī2Ϊ�����������ϵ缫��ӦʽΪ��NO-3e-+2H2O=NO3-+4H+���ʴ�Ϊ��2��NO-3e-+2H2O=NO3-+4H+��
��1molNO�ŵ�����1molNH4+��ת��5mol���ӣ�1molNO������������������ӣ�ת��3mol���ӣ����ݵ�ʧ�����غ㣬���ɵ���������ӵ����ʵ�������笠����ӣ���ϵ缫��Ӧʽ��Ϊʹ��������ȫת��ΪNH4NO3����Ҫ���䰱�����ʴ�Ϊ��NH3��
(2)�ٸ���ͼ֪�����ʱ�������е缫�������ӷŵ�����������������Ϊ�����ң���ӵ�Դa��Ϊ���������ҷ����ĵ缫��ӦʽΪ2H++2e- = H2��������Ϊ�����ң�������ͨ����ǵ���������ɵ������ᣬ���������ϵ�������ʧ���Ӻ�ˮ�������ᣬ�缫��ӦʽΪNO2-e-+H2O=NO3-+2H+���ʴ�Ϊ������2H++2e- = H2����
��n(NO2)=![]() =0.1mol��������ӦʽΪNO2-e-+H2O=NO3-+2H+����0.2mol���������ɣ���Ϊ��0.1mol�������ɣ�����0.1mol������ͨ�����ӽ���Ĥ���������ң��ʴ�Ϊ��0.1��
=0.1mol��������ӦʽΪNO2-e-+H2O=NO3-+2H+����0.2mol���������ɣ���Ϊ��0.1mol�������ɣ�����0.1mol������ͨ�����ӽ���Ĥ���������ң��ʴ�Ϊ��0.1��
�۱�״����28L H2�����ʵ���n(H2)=![]() =1.25mol��ת�Ƶ��ӵ����ʵ���=1.25mol��2=2.5mol�����������Һ��������1 mol HNO3��0.1 mol HNO2��˵������������1mol HNO3��0.1molHNO2���ɣ�����Nԭ���غ��n(NO)+n(NO2)=1mol+0.1 mol=1.1 mol������0.1mol������ת�Ƶ���0.1mol������������ת�Ƶ������ʵ���=2.5mol-0.1mol=2.4mol���跴Ӧ���������NO���ʵ���Ϊxmol���������������ʵ���Ϊymol������Nԭ���غ㼰ת�Ƶ����غ�ã�x+y=1.1-0.1��3x+y=2.4�����x=0.7��y=0.3��n(NO)��n(NO2)=(0.7+0.1)mol��0.3mol=8��3����ͬ��������������֮�ȵ������ʵ���֮�ȣ�����NO�Ͷ������������֮��Ϊ8��3���ʴ�Ϊ��8��3��
=1.25mol��ת�Ƶ��ӵ����ʵ���=1.25mol��2=2.5mol�����������Һ��������1 mol HNO3��0.1 mol HNO2��˵������������1mol HNO3��0.1molHNO2���ɣ�����Nԭ���غ��n(NO)+n(NO2)=1mol+0.1 mol=1.1 mol������0.1mol������ת�Ƶ���0.1mol������������ת�Ƶ������ʵ���=2.5mol-0.1mol=2.4mol���跴Ӧ���������NO���ʵ���Ϊxmol���������������ʵ���Ϊymol������Nԭ���غ㼰ת�Ƶ����غ�ã�x+y=1.1-0.1��3x+y=2.4�����x=0.7��y=0.3��n(NO)��n(NO2)=(0.7+0.1)mol��0.3mol=8��3����ͬ��������������֮�ȵ������ʵ���֮�ȣ�����NO�Ͷ������������֮��Ϊ8��3���ʴ�Ϊ��8��3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ����ۺ�������(SPFS)��һ����Ҫ�����߷�������������������ˮ����Ϊ��ҵ��������ˮ���������������Ҫ��Ӧ�á�SPFS�ɱ�ʾ��Fex(OH)y(SO4)z��nH2O����ҵ�ϳ��õ�һ���Ʊ�����Ϊ��(�̷���ѧʽΪFeSO4��7H2O)
![]()
��SPFS�Ķ������ָ���У��λ�������Ҫ������ָ��֮һ���λ��ȶ���Ϊ���λ��ȣ�n(OH��)/3n( Fe) ��100%��ʽ��n��OH������n(Fe)�ֱ��ʾ����ۺ���������OHһ��Fe�����ʵ������Իش��������⡣
��1�����̷��м������Խ��ʵ�NaClO3Ŀ����__________ ��
��2��SPFS����ˮ����ˮ��Ӧ����__________ ������ˮ�е�������������ˮ��
��3��ȡ15.05gij����ۺ��������ܽ���ˮ�������м��˹�����BaCI2��Һ��������ȫ�������ˡ�ϴ�ӡ�����ð�ɫ����20.97g.��������Һ�м���NH3H2O��������ҺpH= 6�������ˡ�ϴ�ӡ������Fe2O3����5.60g���ù���ۺ����������λ���Ϊ_________ ��
��4��������ù���ۺ���������Ʒ�Ļ�ѧʽ______________(д���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() Ϊ�����ӵ�������ֵ������˵����ȷ����
Ϊ�����ӵ�������ֵ������˵����ȷ����![]()
A.![]() �����������۳�ַ�Ӧת�Ƶĵ�����Ϊ
�����������۳�ַ�Ӧת�Ƶĵ�����Ϊ![]()
B.32g���������������г��ȼ�գ�ת�Ƶ�����Ϊ![]()
C.![]() ��Һ������
��Һ������![]() ����ĿΪ
����ĿΪ![]()
D.![]() ��
��![]() �Ĺ��������к��е���������Ϊ
�Ĺ��������к��е���������Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ò��缫���CuSO4��Al2(SO4)3�Ļ��Һһ��ʱ�������Һ�м���0.5mol Cu2(OH)2 CO3ǡ��ʹ��Һ��ԭ���������ת�Ƶĵ��ӵ����ʵ���Ϊ( ����)
A.1 molB.2 molC.3 molD.4 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����![]()
A.�����ƺ�������������ɱ�����ú����
B.ʪ��ұ����ָ��������Һ�з������û���Ӧ����������û�������ͭ��Һ�е�ͭ
C.�ò�˿պȡ����ij��Һ������ɫ��Ӧ������ʻ�ɫ������Һһ����������Һ
D.�Ʊ�![]() ��
��![]() ��
��![]() �����ܲ��ý���Һֱ�����ɵķ���
�����ܲ��ý���Һֱ�����ɵķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɻ�������Ƶ�1,2��������������Ӧ�������£�

����˵����������
A. �ٵķ�Ӧ�����ǹ��� B. �ڵķ�Ӧ��������ȥ��Ӧ
C. �۵ķ�Ӧ������ȡ����Ӧ D. �ܵķ�Ӧ������NaOH��H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����1����H2O2��H2SO4�Ļ����Һ���ܳ�ӡˢ��·�������ĩ�е�ͭ��д����Ӧ�����ӷ���ʽ��_______________________��
��2����������������ͬ��ӡˢ��·��Ľ�����ĩ��10%H2O2��3.0 mol/L��H2SO4�����Һ��������ò�ͬ�¶���ͭ��ƽ���ܽ�����(���±�)��
�� ��(T) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
ͭƽ���ܽ�������10-3mol��L-1��min-1 | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
���¶ȸ���40��ʱ��ͭ��ƽ���ܽ��������ŷ�Ӧ�¶����߶��½�������Ҫԭ����________________________________________________��
��3�����ᴿ���CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ�����ȣ�����CuCl�������Ʊ�CuCl�����ӷ���ʽ��_________________________________________��
II��������ˮ�е��͵���Ҫ�������κ������ʽ���ڡ�
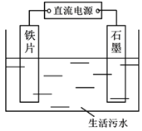
��1������ԭ������ͼ��ʾ�����õ�ⷨ��PO43-ת��ΪFe3��PO4��2������ȥ������___________������������������������û�ѧ�����ʾ����Fe2+����Ҫ���̣�__________________________��
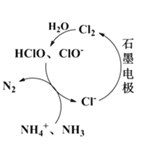
��2����Cl-����ʱ������ԭ����ͼ��ʾ����Ҫ��������������Ч�ȣ�HClO��ClO-����NH4+��NH3����ΪN2����pH��7ʱ����Ҫ����HClO����NH4+�ķ�Ӧ�������ӷ���ʽΪ��_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������У�������Һ�ĵ��������仯�������
A. ![]() ��Һ�е���
��Һ�е���![]() ��Һ������
��Һ������
B. ������Һ�е��백ˮ������
C. ����ʯ��ˮ��ͨ��![]() ������
������
D. ![]() ��Һ�м���������NaOH����
��Һ�м���������NaOH����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com