
| A. | 1mol金属钠含有的电子数 | |
| B. | 1L 1mol/L硫酸溶液所含的H+数 | |
| C. | 标准状况下,22.4L四氯化碳所含的分子数 | |
| D. | 0.012kg12C所含的原子数 |
分析 A.钠原子含有11个电子,1mol钠原子中含有11mol电子;
B、先计算出硫酸的物质的量,1mol硫酸在溶液中电离出2mol氢原子;
C、标准状况下,22.4L四氯化碳的物质的量不是1mol;
D、根据国际规定1mol来回答.
解答 解:A.1mol钠原子中含有11mol电子,不能表示阿伏加德罗常数数值,故A错误;
B.1 L 1 mol•L-1硫酸溶液中含有1mol硫酸,1mol硫酸在溶液中电离出2mol氢离子,不能表示阿伏加德罗常数数值,故B错误;
C.标况下四氯化碳不是气体,22.4L四氯化碳的物质的量不是1mol,不能表示阿伏加德罗常数数值,故C错误;
D.国际规定:0.012kg12C所含的原子数为阿伏伽德罗常数个碳原子,能表示阿伏加德罗常数数值,故D正确;
故选D.
点评 本题考查阿伏加德罗常数,题目难度不大,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确阿伏伽德罗常数的概念及表示的意义.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L 的CCl4含有4NA个Cl原子 | |
| B. | 0.1 mol•L-1Na2S溶液中含有0.1NA个S2- | |
| C. | 常温常压下,92g的NO2和N2O4混合气体含有的N原子数为2NA | |
| D. | 常温常压下,22.4L氯气与足量的铁粉反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2参加化学反应获得的电子数都是2NA | |
| B. | 6.4 gO2与O3的混合物中所含O原子数一定为0.4NA | |
| C. | 含4nmol HCl的浓盐酸与足量的MnO2加热反应,生成的Cl2分子数为nNA | |
| D. | 1mol某气体的体积为22.4L,该气体的状况一定是标准状况 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
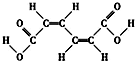
| A. | 该物质有三种3种不同化学环境的氢(不考虑顺反异构) | |
| B. | 1mol该有机物可以和2mol NaOH反应,但不能用Na2CO3溶液区分该有机物和CH3COOCH2CH3 | |
| C. | 该有机物能发生加成反应不能发生取代反应 | |
| D. | 该有机物与乙酸互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15mol•L-1 | B. | 0.3mol•L-1 | C. | 0.45mol•L-1 | D. | 0.2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na投入到足量的盐酸中:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 三氯化铁溶液中加入铜粉:Fe3++Cu═Fe2++Cu2 | |
| D. | 将氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机物都能燃烧生成二氧化碳和水,且受热不易分解 | |
| B. | 有机物大多数难溶于水而易溶于汽、四氯化碳等有机溶剂 | |
| C. | 有机物都是非电解质且熔点、沸点较低 | |
| D. | 有机化学反应都较复杂,且副反应多,反应速率慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com