
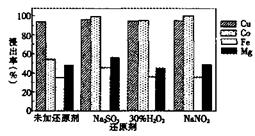
水钴矿(含Cu0、C0203 ,Fe2O3、MgO等)用硫酸法浸出铜和钴,下图是不同还原剂对元素浸 出率的影响(硫酸浓度3 mol•L-1,温度60 0C),下列说法正确的是
 A. 是否使用还原剂对铜的浸出率影响很大
A. 是否使用还原剂对铜的浸出率影响很大
B. 用Na2SO3和NaNO2作还原剂,钴的浸出率均达98%。但工业上宜选用Na2SO3
C.加入还原剂的主要目的是为了还原Fe3+
D.用Na2SO3作还原剂可使镁元素以单质形式析出而有较大浸出率
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中Cl-、Br-、I-的物质的量之比为4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的( )
A.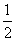 B.
B.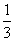
C.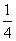 D.
D.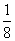
查看答案和解析>>
科目:高中化学 来源: 题型:
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中单质铁的物质的量为
A. mol B.
mol B.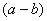 mol C.
mol C. mol D.
mol D. 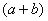 mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期律,下列推断正确的是
A.酸性:H2SiO3>H2CO3 B.热稳定性:H2Se>H2S>H2O
C.碱性:CsOH>Ca(OH)2 D.若离子半径:R2->M+,则原子序数:R >M
查看答案和解析>>
科目:高中化学 来源: 题型:
制烧碱所用盐水需两次精制。第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水。
(1)过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
①检测Fe3+是否除尽的方法是________________________________________。
②过程Ⅰ选用BaCl2而不选用CaCl2,运用表中数据解释原因____________________。
③检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测_______(填离子符号)。
(2)第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:
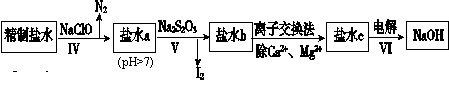

①过程Ⅳ除去的离子是________________。
②过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将足量CO2气体通入水玻璃中,然后加热蒸干,再在高温下充分灼烧,最后所得的固体物质是( )
A.Na2SiO3 B.Na2CO3、Na2SiO3
C.Na2CO3、SiO2 D.SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属元素特征的叙述正确的是( )
A.金属元素的原子只有还原性,离子只有氧化性
B.金属元素在化合物中一定显正价
C.金属元素在不同化合物中化合价均不同
D.金属单质在常温下均是固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com