
(1)��Bԭ����ͬ��Ԫ����ԭ�Ӱ뾶��Сʱ����AԪ��Ϊ___________________��BԪ��Ϊ____________��AB��ѧʽΪ________________��
(2)��B��������Ԫ�صĺ˵����������˳��4��AB�ͻ�����Ļ�ѧʽ����Ϊ___________��________________��________________��________________�����з����м��ļ�����ǿ��Ӧ��____________����������ȵ����ʵ������ڵ�����ˮ�У�������Һ������ǿ����________________��������������____________��
������(1)A2��B2����˫ԭ�ӷ��ӣ�Ԥ������Ӧ������̬���ӣ�AB�ǹ��ۻ����AB��AԪ�������ۣ�����+1�ۣ���ΪHԪ�أ�Bԭ����ͬ����ԭ�Ӱ뾶��Сʱ��BΪFԪ�ء�
(2)B��������Cl��Br��IԪ��֮һ������Ҳ������H�γ�AB���ۻ����
(3)HF��HCl��HBr��HI�У�F�ķǽ�������ǿ���������ӵ�������ǿ��HF�����й��õ��Ӷ�ƫ��Hԭ�ӵij̶����H��F��������ǿ��
HX(X����±��)ˮ��Һ�����ԣ���Xԭ�����������Ӷ���ǿ������HI(aq)��������ǿ��HF(aq)������������������������ᣬ������±�ᶼ��ǿ�ᡣ
�𰸣�(1)H F HF
(2)HF HCl HBr HI HF HI HF


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
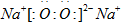
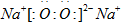
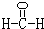
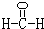
| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | ���ʻ�ԭ�ӽṹ |
| A | ԭ�Ӻ���ֻ��һ������ |
| B | �����ǿ����к����������� |
| X | ԭ�ӵ������������Ǵ�����������3�� |
| Y | ������Ԫ����ԭ�Ӱ뾶����Ԫ�� |
| Z | ��������ϼ���������ϼ۵Ĵ�����Ϊ6 |
| ||
| ���¸�ѹ |
| ||
| ���¸�ѹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | ���ʻ�ԭ�ӽṹ |
| A | ԭ�Ӻ���ֻ��һ������ |
| B | �����ǿ����к����������� |
| X | ԭ�ӵ������������Ǵ�����������3�� |
| Y | ������Ԫ����ԭ�Ӱ뾶����Ԫ�� |
| Z | ��������ϼ���������ϼ۵Ĵ�����Ϊ6 |
| ||
| �� |
| ||
| �� |
| ʵ����� | ʵ������ | ���ۼ����� |
| ��ȡ����NaBr ��Һ���Թ��У��μ� ��ˮ ��ˮ �������ټ�������CCl4�������ã� |
����Һ����ɫ��Ϊ�Ȼ�ɫ�� ����Һ�ֲ㣬 �ϲ�Һ�弸��Ϊ��ɫ���²�Һ��Ϊ�Ⱥ�ɫ �ϲ�Һ�弸��Ϊ��ɫ���²�Һ��Ϊ�Ⱥ�ɫ �� |
�����ԣ�Z ���ʣ�Br2 ���ӷ���ʽ Cl2+2Br-�T2Cl-+Br2 Cl2+2Br-�T2Cl-+Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
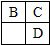 A��B��C��D��E��Ϊ����������Ԫ�أ�B��C��D�����ڱ��е�λ�ù�ϵ��ͼ��ʾ��A�Ƕ�������ԭ�Ӱ뾶��С��Ԫ�أ�A��B��C����Ԫ�ص�ԭ������֮�͵���DԪ�ص�ԭ��������E�Ƕ�����������õĽ���Ԫ�أ�����˵��������ǣ�������
A��B��C��D��E��Ϊ����������Ԫ�أ�B��C��D�����ڱ��е�λ�ù�ϵ��ͼ��ʾ��A�Ƕ�������ԭ�Ӱ뾶��С��Ԫ�أ�A��B��C����Ԫ�ص�ԭ������֮�͵���DԪ�ص�ԭ��������E�Ƕ�����������õĽ���Ԫ�أ�����˵��������ǣ�������| A�������ӵİ뾶��С��ϵ��B��C��E | B��CԪ�ص���̬�⻯���DԪ�ص���̬�⻯���ȶ��������Ե�� | C����A��B����Ԫ����ɵ����ӻ�����NH5�У����������Ӹ�����Ϊ1��1 | D����C��D��E����Ԫ����ɵ�ij�ֻ������ˮ��Һ�������ᷴӦ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com