
分析 0.1mol烃与22.4升标准状况下的O2(过量)混合,完全燃烧后为CO2、H2O、O2(剩余)混合气体,混合气体通过足量的Na2O2固体,发生反应2CO2+2Na2O2=2Na2CO3+O2,Na2O2增重相当于与CO2等物质的量的CO的质量,发生反应2H2O+2Na2O2=4NaOH+O2,Na2O2增重相当于烃中H元素质量,从Na2O2中溢出的全部气体为16.8L(标况)为氧气,水中的氧元素完全转移到氧气中,反应2CO2+2Na2O2=2Na2CO3+O2导致整个过程中氧气的物质的量减小,根据氧气物质的量减少可以计算CO2的物质的量,再结合过氧化钠质量增重计算H元素的质量,根据原子守恒进而确定化学式.
解答 解:0.1mol烃与22.4升标准状况下的O2(过量)混合,完全燃烧后为CO2、H2O、O2(剩余)混合气体,混合气体通过足量的Na2O2固体,发生反应2CO2+2Na2O2=2Na2CO3+O2,Na2O2增重相当于与CO2等物质的量的CO的质量,发生反应2H2O+2Na2O2=4NaOH+O2,Na2O2增重相当于烃中H元素质量,从Na2O2中溢出的全部气体为16.8L(标况)为氧气,水中的氧元素完全转移到氧气中,反应2CO2+2Na2O2=2Na2CO3+O2导致整个过程中氧气的物质的量减小,
从Na2O2中溢出的全部气体为16.8L(标况)为氧气,其物质的量=$\frac{16.8L}{22.4L/mol}$=0.75mol,故整个过程中氧气物质的量减少1mol-0.75mol=0.25mol,则:
2CO2+2Na2O2=2Na2CO3+O2 氧气物质的量减少
2 1
0.5mol 0.25mol
故烃中氢元素的质量=15g-0.5mol×28g/mol=1g,则氢原子物质的量=$\frac{1g}{1g/mol}$=1mol,
则该烃中C原子数目=$\frac{0.5mol}{0.1mol}$=5、H原子数目=$\frac{1mol}{0.1mol}$=10,故该烃的分子式为:C5H10,
答:该烃的分子式为C5H10.
点评 本题考查有机物分子式的确定,关键是根据整个过程中氧气的物质的量变化计算二氧化碳,注意理解差量法的应用,难度较大,侧重于考查学生的分析能力和计算能力.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:解答题
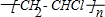 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | 最高价氧化物对应的水化物的酸性:Z<Q | |
| C. | Q和W可形成原子个数比为1:1和2:1的化合物 | |
| D. | X、Y和W三种元素形成的化合物的水溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属Al无剩余 | B. | 有白色沉淀生成 | ||
| C. | 所得气体全部为氢气 | D. | Na的物质的量是0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
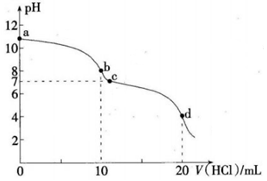
| A. | a、d 两点溶液中水电离出的c(H+):a<d | |
| B. | b点溶液存在:c(CO32-)+c(HCO3-)+c(H2CO3)=0.100mol/L | |
| C. | c点溶液存在:c(Na+)-c(Cl-)=c(HCO3-)+2c(CO32-) | |
| D. | b点溶液加水稀释过程中,溶液的pH不断升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
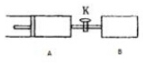 如图所示,向A、B中均充入1mol x、1mol Y,起始过A、B的体积都等于1L.在同温、同压和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0,达平衡时,A的体积为1.4L.下列说法错误的是( )
如图所示,向A、B中均充入1mol x、1mol Y,起始过A、B的体积都等于1L.在同温、同压和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0,达平衡时,A的体积为1.4L.下列说法错误的是( )| A. | 两容器中的反应分别达到平衡时,反应物X的速率:v(B)>v(A) | |
| B. | A容器中x的转化率为80% | |
| C. | 平衡时的压强:PA<PB | |
| D. | 平衡时Y体积分数:A>B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com