
【题目】下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJmol-1
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJmol-1,则1/2H2SO4(aq)+1/2Ba(OH)2(aq)═1/2BaSO4(s)+H2O(l) △H = -57.3kJmol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H = -38.6kJmol-1
2NH3(g) △H = -38.6kJmol-1
D. 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O2比O3稳定
【答案】D
【解析】
甲烷的燃烧热是1mol甲烷完全燃烧生成二氧化碳和液态水放出的热量;H2SO4(aq)与Ba(OH)生成水和硫酸钡沉淀,所以0.5molH2SO4(aq)与0.5molBa(OH)2(aq)反应放出热量大于57.3kJ;合成氨反应可逆,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g)的物质的量小于1mol;根据盖斯定律:3O2(g)═2O3(g)△H=-2834.9kJmol-1-(-3119.1KJmol-1)=284.1KJ/mol,所以氧气能量小于臭氧;
甲烷的燃烧热是1mol甲烷完全燃烧生成二氧化碳和液态水放出的热量,甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(l) △H = -890.3kJmol-1,故A错误 ;H2SO4(aq)与Ba(OH)生成水和硫酸钡沉淀,所以0.5molH2SO4(aq)与0.5molBa(OH)2(aq)反应放出热量大于57.3kJ,故B错误;合成氨反应可逆,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g)的物质的量小于1mol,所以N2(g) + 3H2(g)![]() 2NH3(g) △H < -38.6kJmol-1,故C错误 ;根据盖斯定律:3O2(g)═2O3(g)△H=-2834.9kJmol-1-(-3119.1KJmol-1)=284.1KJ/mol,所以氧气能量小于臭氧,所以O2比O3稳定,故D正确。
2NH3(g) △H < -38.6kJmol-1,故C错误 ;根据盖斯定律:3O2(g)═2O3(g)△H=-2834.9kJmol-1-(-3119.1KJmol-1)=284.1KJ/mol,所以氧气能量小于臭氧,所以O2比O3稳定,故D正确。


科目:高中化学 来源: 题型:
【题目】质量分数为90%的硫酸溶液和质量分数为10%的硫酸溶液等体积混合后溶质的质量分数
A. 大于50%
B. 等于50%
C. 小于50%
D. 不能做上述估计
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃相对分子质量为86,若该分子中仅含有3个甲基(—CH3),则其一氯取代物最多有( )种(不考虑立体异构)
A. 7 B. 8 C. 9 D. 10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲池是以甲醇为原料,KOH为电解质的高效燃料电池,电化学过程的如图。
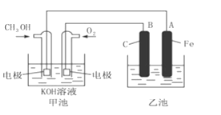
下列说法中不正确的是
A. 甲池的总反应式为:2CH3OH+3O2+4KOH== 2K2CO3+6H2O
B. 若乙池中为足量AgNO3溶液,则阳极的电极反应为4OH--4e- = 2H2O+O2↑
C. 若乙池中为一定量CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为0.2NA
D. 常温常压下,1 g CH3OH燃料生成CO2和液态H2O时放热22.68 kJ,表示该反应的热化学方程式为CH3OH(l)+1.5O2(g) ==CO2(g)+2H2O(l) ΔH= -725.80 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 将1molCl2通入足量水中,溶液中HC1O、Cl-、ClO-粒子数之和为2NA
B. 100 g CaCO3晶体和136 g KHSO4晶体中含有的离子数分别为2 NA 和3 NA
C. 3mol Fe在纯氧中完全燃烧转移的电子数为8NA
D. 已知:N2(g)+3H2(g) ![]() 2NH3 (g) ΔH=-92 kJ·mol-1,当有46 kJ热量放出时,形成NA个共价键
2NH3 (g) ΔH=-92 kJ·mol-1,当有46 kJ热量放出时,形成NA个共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲容器中进行如下反应4A(s)+3B(g)![]() 2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的下列说法正确的是
2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的下列说法正确的是
A. 在2 min末的反应速率,用B表示是 0.3 mol/(L·min)
B. 用A表示的反应速率是0.4 mol/(L·min)
C. 若乙容器中也同时进行此反应,且相同时间段内用D表示的速率是0.2 mol/(Lmin),则乙容器中反应速率更快
D. 对甲容器升高温度,则正反应速率将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁和高铁酸钾都是常见的水处理剂。某兴趣小组以铁屑为原料模拟工业上制备氯化铁及进一步氧化制备高铁酸钾的流程如下:

请回答下列问题:
(1)“氧化”阶段通入过量空气比用氯气作氧化剂具有的优点是__________________________________。
(2)“合成”阶段生成Na2FeO4的离子方程式为__________________________________。
(3)为了检验“氧化”过程中所得FeCl3溶液中是否含有Fe2+,某同学取少量溶液于试管中,选用下列试剂可以达到目的的是_______(填字母)。
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液
若选用酸性K MnO4溶液进行检验,请分析方案是否合理,并说明理由:_____________________________。
(4)过程①制取FeCl3固体的具体操作步骤是_____________________________________________________。若使6.4mol/LFeCl3饱和溶液不析出Fe(OH)3,需控制溶液的pH小于_______{已知该实验条件下,Ksp[(Fe(OH)3]=8.5×10-36,Kw=1.1×10-13,1.13≈1.33}
(5)在不同温度和不同pH下,FeO42-的稳定性如下图所示:

从上图分析,为了提高“合成”阶段Na2FeO4的产率,可采取的实验条件范围为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(H2 NCOONH4)是一种白色晶体,是常见的实验药品,可由干燥的NH3和干燥的CO2在任何比例下反应得到每生成1.0g氨基甲酸铵放出2.05kJ的热量。回答下列问题:
(1)实验室可选用下列装置(I~V)制备干燥的NH3和CO2。
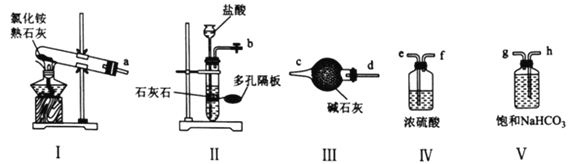
①用装置I、Ⅲ制备并纯化NH3时,接口a与________________(填接口字母)相连,装置I中发生反应的化学方程式为________________________。
②制备并纯化CO2时,按气流从左至右的方向,各接口连接顺序为________________(填接口字母)
(2)一种制备氨基甲酸铵的改进实验装置如下图所示:
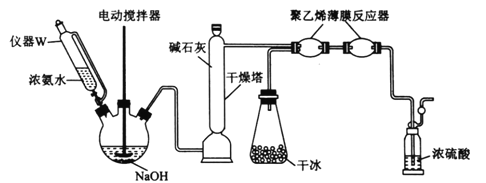
①用仪器W代替分液漏斗的优点是________________________;用干冰装置代替(1)中制备并纯化CO2装置的优点是________________________。
②“薄膜反应器”中发生反应的热化学方程式为________________________;盛浓硫酸的装置的作用是________________________________(列举2点)。
③体系中若有水蒸气,还可能生成的铵盐是________________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= —24.8 kJ·mol-1;3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ·mol-1 ;Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +19.4kJ·mol-1则14g CO气体与足量FeO充分反应得到Fe单质和CO2气体时的释放或吸收的热量为
A. 放出11 kJ B. 放出5.5kJ C. 吸收11 kJ D. 吸收5.5 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com