
| A. | SiO2中含Al2O3杂质,可以加入足量NaOH溶液然后过滤除去 | |
| B. | CO2中含有CO杂质,可以通入盛有CuO的玻璃管且加热 | |
| C. | CO2中含有HCl杂质,可以通过盛有Na2CO3溶液的洗气瓶 | |
| D. | Na2CO3溶液中含有Na2SiO3杂质,可以通入足量的CO2,然后过滤 |
分析 A.二者都与氢氧化钠反应;
B.CO与CuO在加热条件下反应生成CO2;
C.二者都与碳酸钠溶液反应;
D.二者都与二氧化碳反应.
解答 解:A.二者都与氢氧化钠反应,可加入盐酸或稀硫酸除杂,故A错误;
B.CO与CuO在加热条件下反应生成CO2,可用于除去杂质,故B正确;
C.二者都与碳酸钠溶液反应,应用饱和碳酸氢钠溶液除杂,故C错误;
D.二者都与二氧化碳反应,应在反应后的溶液中加入适量的氢氧化钠,再重新生成碳酸氢钠,故D错误.
故选B.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,注意除杂时不能引入新杂质,难度不大.


科目:高中化学 来源: 题型:解答题
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 内容 |  | 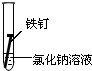 |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、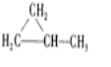 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景.在催化剂作用下可用H2和CO合成甲醇,反应的化学方程式为2H2(g)+CO(g) $\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.试回答下列问题:
甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景.在催化剂作用下可用H2和CO合成甲醇,反应的化学方程式为2H2(g)+CO(g) $\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol O2和4mol NO2 | B. | 1mol NO和4mol NO2 | ||
| C. | 1mol O2和4mol NO | D. | 4mol NO和1mol NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀铜制印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | NH4HCO3溶液和过量的NaOH溶液相混合:HCO3-+OH-═CO32-+H2O | |
| C. | 向Fe2(SO4)3的酸性溶液中通入足量H2S:Fe3++H2S═FeS↓+2H+ | |
| D. | FeI2溶液中通入Cl2至I-恰好完全被氧化:2I-+Cl2═I2+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷与Cl2反应制氯乙烷 | |
| B. | 乙醇和浓硫酸共热制乙烯 | |
| C. | 乙酸和乙醇共热酯化 | |
| D. | 乙烯在催化剂作用下直接氧化制得唯一产物乙醛 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com