
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«µČĮæµÄĘųĢå·Ö±šĶØČėĘšŹ¼Ģå»żĻąĶ¬µÄĆܱÕČŻĘ÷IŗĶ¢ņÖŠ£ØČēĶ¼£©£¬Ź¹Ęä·¢Éś·“Ó¦£¬t0Ź±ČŻĘ÷IÖŠ“ļµ½»ÆŃ§Ę½ŗā£¬X”¢Y”¢ZµÄĪļÖŹµÄĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ŌņĻĀĮŠÓŠ¹ŲĶʶĻÕżČ·µÄŹĒ(”” ””)

A. øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ3X +2Y![]() 3Z
3Z
B. ČōĮ½ČŻĘ÷ÖŠ¾ł“ļµ½Ę½ŗāŹ±£¬Į½ČŻĘ÷µÄĢå»żV£ØI£©<V£Ø¢ņ£©£¬ŌņČŻĘ÷II“ļµ½Ę½ŗāĖłŠčŹ±¼äŠ”ÓŚt0
C. ČōĮ½ČŻĘ÷ÖŠ¾ł“ļµ½Ę½ŗāŹ±£¬Į½ČŻĘ÷ÖŠZµÄĪļÖŹµÄĮæ·ÖŹżĻąĶ¬£¬ŌņYĪŖ¹ĢĢ¬»ņŅŗĢ¬
D. Čō“ļĘ½ŗāŗ󣬶ŌČŻĘ÷¢ņÉżøßĪĀ¶ČŹ±£¬ĘäĢå»ż¼õŠ”£¬ĖµĆ÷Z·¢ÉśµÄ·“Ó¦ĪŖĪüČČ·“Ó¦
”¾“š°ø”æC
”¾½āĪö”æA£®ÓÉĶ¼æÉÖŖ£¬X”¢YµÄĪļÖŹµÄĮæŌö“ó£¬ĪŖÉś³ÉĪļ£¬ZĪļÖŹµÄĮæ¼õŠ”£¬ĪŖ·“Ó¦Īļ£¬µ½Ę½ŗāŗó£¬XÉś³É1.8mol£¬YÉś³É1.2mol£¬Z·“Ó¦1.8mol£¬X”¢Y”¢ZµÄ»Æѧ¼ĘĮæŹżÖ®±Č=1.8£ŗ1.2£ŗ1.8=3£ŗ2£ŗ3£¬Ōņ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ3Z3X+2Y£¬¹ŹA“ķĪó£»B£®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ3Z3X+2Y£¬ČōĮ½ČŻĘ÷ÖŠ¾ł“ļµ½Ę½ŗāŹ±£¬Į½ČŻĘ÷µÄĢå»żV£Ø¢ń£©£¼V£Ø¢ņ£©£¬ŌņČŻĘ÷¢ņ“ļµ½Ę½ŗāŹ±Ģå»żŌö“ó£¬Ń¹Ēæ¼õŠ”µÄ¹ż³Ģ£¬“ļµ½Ę½ŗāĖłŠčŹ±¼ä“óÓŚt0£¬¹ŹB“ķĪó£»C£®ČōĮ½ČŻĘ÷ÖŠ¾ł“ļµ½Ę½ŗāŹ±£¬Į½ČŻĘ÷ÖŠZµÄĪļÖŹµÄĮæ·ÖŹżĻąĶ¬£¬ĖµĆ÷“ļµ½ĻąĶ¬µÄĘ½ŗā£¬²»ŹÜŃ¹ĒæµÄ±ä»ÆÓ°Ļģ£¬ĖłŅŌ·“Ó¦Ē°ŗóĘųĢåĢå»żÓ¦ŹĒ²»±äµÄ·“Ó¦£¬ĖłŅŌYĪŖ¹ĢĢ¬»ņŅŗĢ¬£¬¹ŹCÕżČ·£»D£®Čō“ļĘ½ŗāŗó£¬ČŻĘ÷¢ņŹĒŗćŃ¹ČŻĘ÷£¬ÉżøßĪĀ¶ČŹ±ĘäĢå»żŌö“󣬵«²»ÄÜĖµĆ÷Ę½ŗāÕżĻņ½ųŠŠ£¬Z·¢ÉśµÄ·“Ó¦²»Ņ»¶ØĪŖĪüČČ·“Ó¦£¬¹ŹD“ķĪó£»¹Ź“š°øĪŖC”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ŁÄ³NaClѳʷ֊æÉÄÜŗ¬ÓŠSO42© £¬ CO32© £¬ ĪŖ¼ģŃéŌÓÖŹĄė×ӵēęŌŚ£¬²ÉČ”ČēĻĀŹµŃé²½Öč£ŗ
ѳʷ ![]()
![]() ĪŽĆ÷ĻŌĻÖĻó
ĪŽĆ÷ĻŌĻÖĻó ![]() ĪŽĆ÷ĻŌĻÖĻó£®Ōņ¼ÓČėµÄŹŌ¼ĮAĪŖ £¬ BĪŖ£ØĢī»ÆѧŹ½£©£¬øĆĻÖĻóÖ¤Ć÷ѳʷ֊²»ŗ¬ÓŠ £®
ĪŽĆ÷ĻŌĻÖĻó£®Ōņ¼ÓČėµÄŹŌ¼ĮAĪŖ £¬ BĪŖ£ØĢī»ÆѧŹ½£©£¬øĆĻÖĻóÖ¤Ć÷ѳʷ֊²»ŗ¬ÓŠ £®
¢ŚŌŚŗóŠųŹµŃéÖŠŠčŅŖŹ¹ÓĆ450mL0.5molL©1NaClČÜŅŗ£¬ĪŖÅäÖĘøĆÅضČNaClČÜŅŗ½ųŠŠŹµŃ飬ŠčÓĆĶŠÅĢĢģĘ½³ĘČ”NaClg£®
¢ŪÅäÖĘNaClČÜŅŗŹ±£¬Čō³öĻÖĻĀĮŠ²Ł×÷£¬»įŹ¹ÅäÖĘÅضČĘ«øߵďĒ
A£®³ĘĮæŹ±NaClŅŃ³±½ā
B£®ĢģĘ½ķĄĀėŅŃŠāŹ“
C£®¶ØČŻŹ±ø©ŹÓæĢ¶ČĻß
D£®¶ØČŻŅ”ŌČŗóŅŗĆęĻĀ½µ£¬ÓÖ¼ÓĖ®ÖĮæĢ¶Č£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĮ£×ÓÖŠŹōÓŚĶ¬Ī»ĖŲµÄŹĒ
A. 16OŗĶ18O B. H2OŗĶH2O2 C. 19KŗĶ20Ca D. O2ŗĶO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņ»Æ¼ī·ØŹĒ¹¤ŅµÉĻÖʱøNa2S2O3µÄ·½·ØÖ®Ņ»£¬·“Ó¦ŌĄķĪŖ£ŗ2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2£ØøĆ·“Ó¦”÷H£¾0£©”£Ä³ŃŠ¾æŠ”×éŌŚŹµŃéŹŅÓĆĮņ»Æ¼ī·ØÖʱøNa2S2O3”¤5H2OĮ÷³ĢČēĻĀ”£

£Ø1£©ĪüĮņ×°ÖĆČēĶ¼ĖłŹ¾”£

¢Ł×°ÖĆBµÄ×÷ÓĆŹĒ¼ģŃé×°ÖĆAÖŠSO2µÄĪüŹÕŠ§ĀŹ£¬BÖŠŹŌ¼ĮŹĒ_____________£¬±ķĆ÷SO2ĪüŹÕŠ§ĀŹµĶµÄŹµŃéĻÖĻóŹĒBÖŠČÜŅŗ______________”£
¢ŚĪŖĮĖŹ¹SO2¾”æÉÄÜĪüŹÕĶźČ«£¬ŌŚ²»øıäAÖŠČÜŅŗÅØ¶Č”¢Ģå»żµÄĢõ¼žĻĀ£¬³żĮĖ¼°Ź±½Į°č·“Ó¦ĪļĶā£¬»¹æɲÉČ”µÄŗĻĄķ“ėŹ©ŹĒ______________”££ØČĪŠ“Ņ»Ģõ£©
£Ø2£©¼ŁÉč±¾ŹµŃéĖłÓƵÄNa2CO3ŗ¬ÉŁĮæNaCl”¢NaOH£¬Éč¼ĘŹµŃé·½°ø½ųŠŠ¼ģŃ锣£ØŹŅĪĀŹ±CaCO3±„ŗĶČÜŅŗµÄpH£½10.2£©£¬ĻŽŃ”ŹŌ¼Į¼°ŅĒĘ÷£ŗĻ”ĻõĖį”¢AgNO3ČÜŅŗ”¢CaCl2ČÜŅŗ”¢·ÓĢŖČÜŅŗ”¢ÕōĮóĖ®”¢pH¼Ę”¢ÉÕ±”¢ŹŌ¹Ü”¢µĪ¹Ü
ŠņŗÅ | ŹµŃé²Ł×÷ | Ō¤ĘŚĻÖĻó | ½įĀŪ |
¢Ł | ȔɣĮæѳʷӌŹŌ¹ÜÖŠ£¬¼ÓČėŹŹĮæÕōĮóĖ®£¬³ä·ÖÕńµ“Čܽā£¬____________ ”£ | ÓŠ°×É«³ĮµķÉś³É | ѳʷŗ¬NaCl |
¢Ś | ĮķȔɣĮæѳʷӌÉÕ±ÖŠ£¬¼ÓČėŹŹĮæÕōĮóĖ®£¬³ä·Ö½Į°čČܽā£¬_______”£ | Óė°×É«³ĮµķÉś³É£¬ÉĻ²ćĒåŅŗpH>10.2 | ѳʷŗ¬NaOH |
£Ø3£©Na2S2O3ČÜŅŗŹĒ¶ØĮæŹµŃéÖŠµÄ³£ÓĆŹŌ¼Į£¬²ā¶ØĘäÅØ¶ČµÄ¹ż³ĢČēĻĀ£ŗ
µŚŅ»²½£ŗ×¼Č·³ĘČ”a g KIO3(Ļą¶Ō·Ö×ÓÖŹĮæ£ŗ214)¹ĢĢåÅä³ÉČÜŅŗ£¬
µŚ¶ž²½£ŗ¼ÓČė¹żĮæKI¹ĢĢåŗĶH2SO4ČÜŅŗ£¬µĪ¼ÓÖøŹ¾¼Į£¬
µŚČż²½£ŗÓĆNa2S2O3ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄNa2S2O3ČÜŅŗµÄĢå»żĪŖv mL”£Ōņc(Na2S2O3)£½______mol”¤L-1”££ØÖ»ĮŠ³öĖćŹ½£¬²»×÷ŌĖĖć£©
ŅŃÖŖ£ŗIO3-+I-+6H+=3I2+3H2O 2S2O32-+I2=S4O62-+2I-”£¼×Ķ¬Ń§Ź¢×°Na2S2O3ČÜŅŗÖ®Ē°Ī“ČóĻ“£¬ÕāŃł²āµĆµÄNa2S2O3µÄÅضČæÉÄÜ________£ØĢī”°ĪŽÓ°Ļģ”±”¢”°Ę«µĶ”±»ņ”°Ę«øß”±)£»ŅŅĶ¬Ń§µŚŅ»²½ŗĶµŚ¶ž²½µÄ²Ł×÷¶¼ŗÜ¹ę·¶£¬µŚČż²½µĪĖŁĢ«Āż£¬ÕāŃł²āµĆµÄNa2S2O3µÄÅضČæÉÄÜ________(Ģī”°ĪŽÓ°Ļģ”±”¢”° Ę«µĶ”±»ņ”°Ę«øß”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪŽÉ«ĖįŠŌČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄĄė×Ó×éŹĒ£Ø £©
A. Na+Ӣ K+ӢSO42-ӢCl- B. SO42-ӢCH3COO-ӢAl3+Ӣ Mg2+
C. Cl-ӢFe3+Ӣ K+ӢNa+ D. Na+Ӣ Ba2+ӢCl-ӢHCO3-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓū²ā¶Øŗ¬ÉŁĮæĀČ»ÆÄʵĊ”ĖÕ“ņ¹ĢĢ¬ŃłĘ·ÖŠNaHCO3µÄÖŹĮæ·ÖŹżæɲÉÓĆŅŌĻĀĖÄÖÖ·½·Ø”£
·½·ØŅ»£ŗ

·½·Ø¶ž£ŗ

·½·ØČż£ŗ

·½·ØĖÄ£ŗ²»Ź¹ÓĆ»ÆѧŹŌ¼Į£¬Ź¹ÓĆŹµŃéŹŅ³£ÓĆŅĒĘ÷
°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©·½·ØŅ»£ŗ¼ÓČė×ćĮæµÄŹŌ¼ĮA £ØĢīŠ“AµÄ»ÆѧŹ½£©æɽ«HCO3”Ŗ Ąė×Ó×Ŗ»ÆĪŖ³Įµķ²¢³ĘÖŲ”£²Ł×÷1”¢2”¢3”¢4µÄĆū³ĘŅĄ“ĪŹĒČܽā”¢ ”¢Ļ“µÓŗĶøÉŌļ£ØŗęøÉ£©£»
£Ø2£©·½·Ø¶ž£ŗŌŚ²Ł×÷1ÖŠĖłÓƵ½µÄ²£Į§ŅĒĘ÷ÖŠ£¬³żĮĖÉÕ±”¢²£Į§°ō”¢½ŗĶ·µĪ¹ÜĶā£¬»¹ŠčŅŖµÄÓƵ½µÄŹĒ £¬ŌŚ²Ł×÷2֊ӦєŌń¼×»ł³ČÖøŹ¾¼Į£®
£Ø3£©ŌŚ·½·Ø¶žÖŠ¼ĘĖćøĆѳʷ֊NaHCO3µÄÖŹĮæ·ÖŹżĪŖ [ÓĆĮ÷³ĢĶ¼ÖŠµÄŹż¾Żm”¢V(HCl) ĢīŠ“ÓŠ¹ŲµÄ±ķ“ļŹ½]£»
£Ø4£©ŌŚ·½·ØČżÖŠ£ŗøł¾ŻĖłÓƵďµŃé×°ÖĆ£¬³żĮĖ³ĘĮæŹŌŃłÖŹĮæĶā£¬»¹Šč²ā¶ØµÄŹµŃ鏿¾ŻŹĒ £»
£Ø5£©×ŠĻø·ÖĪö·½·ØČżÖŠµÄŹµŃé×°ÖĆ£¬ČōÓÉ“Ė²āµĆµÄŹż¾ŻĄ“¼ĘĖ揵Ńé½į¹ū£¬ŌņÓŠæÉÄÜĘ«øßŅ²ÓŠæÉÄÜĘ«µĶ£¬Ę«øßµÄŌŅņæÉÄÜŹĒ £¬Ę«µĶµÄŌŅņæÉÄÜŹĒ £Ø¾łĪÄ×Ö¼ņŹö£©£»
£Ø6£©·½·ØĖĵďµŃéŌĄķŹĒ£ŗ £ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗŌŚ¼īŠŌĢõ¼žĻĀ£¬¹ūĢĒÖŠµÄōČ»ł»į×Ŗ»ÆĪŖČ©»ł£¬Ōņ¼ų±š¹ūĢĒÓėĘĻĢŃĢĒµÄŹŌ¼ĮÕżČ·µÄŹĒ
A.äåĖ®B.ŠĀÖĘCu(OH)2Šü×ĒŅŗ
C.ŠĀÖĘŅų°±ČÜŅŗD.Ć¾·Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ·“Ó¦11P+15CuSO4+24H2OØT5Cu3P+6H3PO4+15H2SO4 ÖŠ£¬ŅŃÖŖCu3P ÖŠPĪŖ©3¼Ū£¬Ōņ15mol CuSO4æÉŃõ»ÆµÄPµÄĪļÖŹµÄĮæĪŖ£Ø £©
A.1.5 mol
B.5.5 mol
C.3 mol
D.2.5 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÉÄę·“Ó¦mA(s)+nB(g)![]() eC(g)+fD(g)·“Ó¦¹ż³ĢÖŠ£¬µ±ĘäĖūĢõ¼ž²»±äŹ±£¬CµÄĢå»ż·ÖŹż(C)ŌŚ²»Ķ¬ĪĀ¶Č(T)ŗĶ²»Ķ¬Ń¹Ēæ(P)µÄĢõ¼žĻĀĖꏱ¼ä(t)µÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
eC(g)+fD(g)·“Ó¦¹ż³ĢÖŠ£¬µ±ĘäĖūĢõ¼ž²»±äŹ±£¬CµÄĢå»ż·ÖŹż(C)ŌŚ²»Ķ¬ĪĀ¶Č(T)ŗĶ²»Ķ¬Ń¹Ēæ(P)µÄĢõ¼žĻĀĖꏱ¼ä(t)µÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
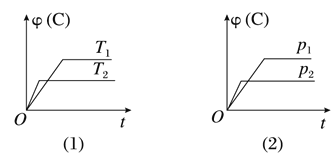
A. “ļµ½Ę½ŗāŗó£¬ČōŹ¹ÓĆ“ß»Æ¼Į£¬CµÄĢå»ż·ÖŹż½«Ōö“ó
B. µ±Ę½ŗāŗó£¬ČōĪĀ¶ČÉżøߣ¬»ÆŃ§Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
C. »Æѧ·½³ĢŹ½ÖŠ£¬n£¾e+f
D. “ļµ½Ę½ŗāŗó£¬Ōö¼ÓAµÄÖŹĮæÓŠĄūÓŚ»ÆŃ§Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com